1、选择题 下列名词中,不属于物理量的是(? )
A.长度
B.质量
C.摩尔
D.时间
参考答案:C
本题解析:摩尔是物质的量的单位,不是物理量,答案选C。
本题难度:简单
2、填空题 实验室要配制250mL?0.8mol?L-1?的NaOH溶液.
(1)需称取NaOH固体的质量为______?g.
(2)在下列仪器中:①托盘天平(带砝码盒);②量筒;③烧杯;④玻璃棒;⑤漏斗;⑥500mL容量瓶;⑦药匙;⑧250mL容量瓶;⑨胶头滴管;⑩坩埚.
A、实验过程中必须用到的仪器有:______(填写代号).?
B、容量瓶使用前应______.
(3)实验时该同学操作步骤如下,请将步骤C补充完整.
A、在烧杯中将已称量好的NaOH用蒸馏水充分溶解;
B、将NaOH溶液沿玻璃棒注入所选的容量瓶中;
C、______;
D、振荡,继续向容量瓶中加水直到液面接近刻度线1-2cm处;
E、改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
F、将容量瓶盖紧,摇匀.
(4)进行操作B前还需注意______;?若不进行C操作,则会使所配溶液浓度______?(填“偏大”、“偏小”或“不变”),若进行E操作时仰视则会使所配溶液浓度______?(同前).
参考答案:(1)需要氢氧化钠的物质的量为0.8mol/L×0.25L=0.2mol,故需要氢氧化钠的质量为0.2mol×40g/mol=8.0g,
故答案为:8.0;
(2)A、配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水),冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,
所以需要的仪器为:①托盘天平(带砝码盒)、③烧杯、④玻璃棒、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、②量筒
(可以可不用),
故答案为:①③④⑦⑧⑨;
B、溶液配制定容后需要反复上下颠倒摇匀,故使用容量瓶之前应检查是否漏水,
故答案为:检查容量瓶是否漏水;
(3)根据溶液配制的步骤可知,C为洗涤烧杯与玻璃棒2~3次,并将洗涤液移入容量瓶内,
故答案为:洗涤烧杯与玻璃棒2~3次,并将洗涤液移入容量瓶内;
(4)氢氧化钠溶解放出大量的热,故移液之前应冷却溶液恢复到室温,
不进行洗涤操作,烧杯壁、玻璃棒上沾有少量的氢氧化钠,移入容量瓶内氢氧化钠的物质的量偏小,所配溶液的浓度偏小,定容时仰视,使液面在刻度线以上,溶液的体积偏大,所配溶液的浓度偏小,
故答案为:冷却溶液恢复到室温;偏小,偏小.
本题解析:
本题难度:一般
3、实验题 (20分)用18.4mol・L-1的浓硫酸,配制 100 ml 1.0 mol・L-1的稀硫酸,请回答以下问题:
(1)需要18.4mol・L-1的浓硫酸 ml。
(2)下列哪组仪器在配制时不需要用到 ( )
①托盘天平 ②分液漏斗 ③250ml容量瓶 ④烧杯 ⑤胶头滴管
⑥量筒 ⑦玻璃棒⑧铁架台(带铁夹) ⑨100ml容量瓶
A.③④⑤⑦⑨ B.①②⑤⑥⑧ C.①②③⑧ D.③④⑤⑥
(3)下列实验步骤中,正确的操作顺序应该是:
A 用量筒量取浓硫酸,缓缓倒入装有约50ml蒸馏水的烧杯里,并用玻璃棒搅拌。
B 用约30ml蒸馏水,分出三次洗涤烧杯和玻璃棒,将每次洗涤液都倒入容量瓶中;
C 将稀释后的硫酸小心地倒入容量瓶中;
D.检查100ml容量瓶瓶口是否有漏液现象;
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1――2cm处;
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,至液面最低点与刻度线相切;
(4)进行A步骤操作的时候,应该选用
①10 ml量筒 ②50 ml量筒 ③5000 ml量筒 ④1000 ml量筒
(5)进行A步操作后,必须 后,才能进行C步操作。
参考答案:(1)5.4
(2)C
(3)D A C B E G F
(4)1
(5)等溶液冷却至室温
本题解析:(1)①密度ρ=1.84g?mL-1,质量分数为98%的浓硫酸的浓度为:c= =18.4mol/L
=18.4mol/L
配制100mL1mol?L-1的稀硫酸,需要该浓硫酸的体积为: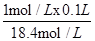 ≈0.0054L=5.4ml,答案:5.4;
≈0.0054L=5.4ml,答案:5.4;
(2)配制100mL1mol/L的稀硫酸的步骤为:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴
签,需要使用的仪器有:烧杯 、量筒 、100mL容量瓶、玻璃棒、定容时必须使用胶头滴管,所以还缺
少的仪器为胶头滴管,不要用到的是①②③⑧,答案选C;
实验过程中先检查容量瓶是否漏液,然后根据计算→量取→稀释、冷却→移液→定容→摇匀→装
瓶→贴签得步骤配置溶液,答案为DACGEBF;
通过计算需要浓硫酸5.4ml,根据选取量筒“大而近”的原则,应选用10ml的量筒,答案选①;
(5)若未冷却到室温即倒入容量瓶中,会使配置硫酸的浓度偏大,答案等溶液冷却到室温;答案:等
溶液冷却至室温
本题难度:一般
4、选择题 科学家刚刚发现了某种元素的原子,其质量是ag,12C的原子质量是bg,NA是阿伏加德罗常数的值,下列说法正确的是
[? ]
A.该原子的摩尔质量是aNA
B.Wg该原子的物质的量一定是bw/aNAmol
C.Wg该原子中含有w/a 个该原子
D.由已知信息可得:NA=12/a
参考答案:C
本题解析:
本题难度:简单
5、填空题 (1)在标准状况下,1.7g氨气所占的体积为__________L,它与标准状况下___________L硫化氢含有相同数目的氢原子。
(2)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____________,R的相对原子质量为__________。
(3)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO______g,所含CO2在标准状况下的体积为__________L。
(4)同温同压下,SO2与氦气的密度之比为________;若质量相同,两种气体的体积比为_____。
参考答案:(16分) (1)2.24 3.36 (2)64g・mol-1 32?(3)2.80 6.72 (4)16∶1?1∶16?(每空2分)
本题解析:略
本题难度:一般