1��ѡ���� ����˵������ȷ����
A.ú�Ǹ��ַ�������ɵĻ����
B.úȼ��ʱ��������������������������̼����������̳�����Ⱦ��
C.ú���Ե���̼Ϊ���ĸ��ӻ����
D.��úΪ��Ҫԭ�ϣ��������Ժϳɼ״��������Լӹ��ɸ�����
�ο��𰸣�BD
���������ú���ɸ��ӵ�������л�����ɣ�����Ҫ����CԪ���⣬������H��O��S��N��Ԫ�أ�������̼���ʺͼ��л�����A��C�Ǵ���ġ�úȼ�ջ���������Ķ����������Ⱦ�����BD��ȷ��
�����Ѷȣ�����
2������� �������⣩��ˮ�л�ѧ��Դ���ۺϿ������ã����ܵ������ĸ߶����ӣ�Br2��Mg�����ֵ��ʶ����ԴӺ�ˮ����ȡ����ͼΪ��ȡ���ǵ���Ҫ���裺
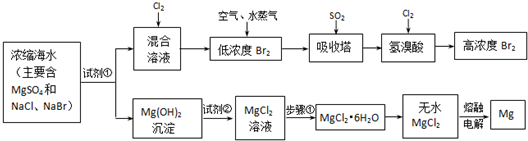
��ش�
�Ӻ�ˮ����ȡ����ռ�������������1/3����Ҫ�����������������еĿ�����������
��1����ȡBr2ʱ��һ��ͨ��Cl2ʱ������Ӧ�����ӷ���ʽ��______��
��2���������з�Ӧ�����ӷ���ʽ��______��
�ɣ�1������2����֪��SO2��Cl2��Br2����������������ǿ������˳����______�����á�������ʾ��
��þ����Ͻ�����;�ܹ�Ľ������ϣ���Ŀǰ������60%��þ���ǴӺ�ˮ�а�����������ȡ�ģ�
��1������������Ϊ��ʹMgSO4��ȫת��ΪMg��OH��2���Լ��ٿ���ѡ��______��д��ѧʽ����
��2�������Լ��ں�Ӧ�����ӷ���ʽ��______��
��3������ٰ������ȡ���������ȴ���ᾧ��______��
��4��ͨ��ʱ��ˮMgCl2������״̬�·�Ӧ�Ļ�ѧ����ʽ��______��
�������������������þ��ͬʱ�������Ƶ������������ʣ������Ʊ��ͻ��������þ�����ᣮ���������ǣ�
�ٽ��Ȼ�þ���壨MgCl2?6H2O�����ȵ�523�����ϣ��þ�����Էֽ�õ��ͻ��������þ��������̬���������һ�����峣����Ϊ��ɫҺ�壮
�ڽ�����������ȴ�����£��ٸ�����Ҫ�����벻ͬ����ˮ���Ϳɵõ���ͬŨ�ȵ����ᣮ
��1��MgCl2?6H2O��523�����Ϸֽ�Ļ�ѧ����ʽ��______��
��2������1molMgCl2?6H2O�ֽ����õķǹ����������ȡ�ܶ�Ϊ1.19g/cm3��������Һ168mL�����ˮ______g����ȷ��0.1���������������ʵ����ʵ���Ũ����______mol/L����ȷ��0.1����
�ο��𰸣�I����1��Ũ����ˮ���Լ��ٷ�Ӧ�õ�������þ��ʣ����Һ�к��е��������ӣ�ͨ�������������������ӷ�Ӧ���ɵ�����������ӣ������ӷ���ʽ��Cl2+2Br-�T2Cl-+Br2��
�ʴ�Ϊ��Cl2+2Br-�T2Cl-+Br2��
��2�������徭��������������������������ͨ��Ķ��������뵥���巴Ӧ��������������ᣬ�仯ѧ����ʽ�ǣ�Br2+SO2+2H2O�T2H2SO4+2HBr���������ӷ���ʽΪBr2+SO2+2H2O�T4H++SO42-+2Br-����������ԭ��Ӧ���������������Ա����������������ǿ������Cl2+2Br-�T2Cl-+Br2�ã�������Cl2��Br2�����ݵ�Br2+SO2+2H2O�T4H++SO42-+2Br-��������Br2��SO2����������ΪCl2��Br2��SO2���ʴ�Ϊ��Br2+SO2+2H2O�T4H++SO42-+2Br-��Cl2��Br2��SO2��
II����1��Ũ����ˮ���Լ��ٷ�Ӧ�õ�������þ�����Լ��ٿ������������ƻ��������ƣ��ʴ�Ϊ��NaOH��
��2��������þ���Լ��ڷ�Ӧ�õ��Ȼ�þ�����Լ��ڱ������ᣬ��Ӧ�Ļ�ѧ����ʽ��Mg��OH��2+2HCl�TMgCl2+2H2O�������ӷ���ʽ��Mg��OH��2+2H+�TMg2++2H2O��
�ʴ�Ϊ��Mg��OH��2+2H+�TMg2++2H2O��
��3��Ҫ���Ȼ�þ��Һ�õ����ᾧˮ���Ȼ�þ������Ҫ��������ȴ���ᾧ����ͨ�����˰ѹ������Һ�з���������ʴ�Ϊ�����ˣ�
��4���������״̬����ˮ�Ȼ�þ���Եõ�������þ���ʣ���MgCl2�����ڣ����.Mg+Cl2�����ʴ�Ϊ��MgCl2�����ڣ����.Mg+Cl2����
III����1����������MgCl2?6H2O��523�����Ϸֽ⣬ʵ������MgCl2?6H2O����ʧˮ�γ��Ȼ�þ��Һ���Ȼ�þˮ������������þ���Ȼ��⣬Ȼ��������þ�����·ֽ�õ�����þ����MgCl2?6H2O��523�����Ϸֽ�õ���Ӧ��������þ���Ȼ����ˮ���仯ѧ����ʽ��MgCl2?6H2O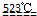 MgO+2HCl��+5H2O�����ʴ�Ϊ��MgCl2?6H2O
MgO+2HCl��+5H2O�����ʴ�Ϊ��MgCl2?6H2O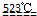 MgO+2HCl��+5H2O����
MgO+2HCl��+5H2O����
��2���õ��������������1.19g/cm3��168mL�T199.92g������MgCl2?6H2O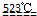 MgO+2HCl��+5H2O����֪��1molMgCl2?6H2O�ֽ�ɵ�2mol�Ȼ��⡢5molˮ�����ߵ�������73g+90g=163g������Ҫ��ˮ��199.92g-163g=36.92g������Ҫ��ˮ36.9g��
MgO+2HCl��+5H2O����֪��1molMgCl2?6H2O�ֽ�ɵ�2mol�Ȼ��⡢5molˮ�����ߵ�������73g+90g=163g������Ҫ��ˮ��199.92g-163g=36.92g������Ҫ��ˮ36.9g��
��Ϊ�������к���2molHCl�����Ϊ0.168L����c��HCl���T2mol0.168L=11.9mol/L���������������ʵ����ʵ���Ũ����11.9mol/L��
�ʴ�Ϊ��36.9g��11.9��
���������
�����Ѷȣ���
3��ѡ���� NaCl�ǴӺ�ˮ����ȡ������һ����Ҫ���ʣ���������ζƷ���⣬������һ����Ҫ�Ļ���ԭ�ϡ����в�Ʒ����������NaClΪ��Ҫԭ����ȡ����
[? ]
�ٽ����ƣ� �������� ���ռ ����� �ݴ���
A��ֻ�Т٢�
B��ֻ�Т٢ڢ�
C��ֻ�Т٢ڢۢ�
D��ȫ��
�ο��𰸣�D
���������
�����Ѷȣ���
4������� ��ˮ�к��зḻ�Ļ�ѧԪ�أ���ͼ��ij���������ú�ˮ������þ�����̼�ͼ����ش�
��1��ʵ����������Ũ��Һ����Ҫ�������в���?�����ƾ��ơ����Ǽܺ�______��
��2����Ӧ���������Լ�Ϊ______��
��3����Ӧ���е���ת��Ϊ______��
��4����Ӧ����ɺ�����еIJ�����______��
��5��B�����к��л�ѧ��Ϊ______��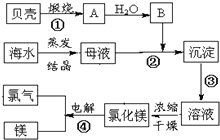
�ο��𰸣���1������������ʵ�������У����������ƾ��ơ����Ǽܺ�������ȣ��ʴ�Ϊ��������
��2�����Լ������Ὣ������þ�ܽ⣬����������þ�����ᷴӦ�����Ȼ�þ��ˮ���ʴ�Ϊ�����
��3�������ǽ�����ת��Ϊ��ѧ�ܵ�װ�ã��ʴ�Ϊ����ѧ�ܣ�
��4��ʵ�ֹ�Һ����ķ����ǹ��ˣ���ˮ�м����������ƺ��Խ�þ���ӳ������������˿��Խ�ĸҺ�ͳ������룬�ʴ�Ϊ�����ˣ�
��5�����������Ǻ������Ӽ����ۼ������ӻ�����ʴ�Ϊ�����Ӽ������ۼ���
���������
�����Ѷȣ�һ��
5������� ��1��ij�л���Ľṹ��ʽΪHO-CH2CH=CHCH2-COOH��д�����л��ﺬ�й�������_______��______��
______�����л�����ܷ����Ļ�ѧ��Ӧ��___________������ţ�
��ˮ�� ������ �ۼӳ� �� ������
�Ӻ�ˮ�п��Ի�õ�ˮ��ʳ�Σ�������ȡþ��������ʡ�
��2����ˮ�����ķ�����Ҫ��____________����һ�֣���
��3���Ӻ�ˮ����ȡ�����Ҫ��������Ũ���ĺ�ˮ��ͨ�����������������������÷�Ӧ�����ӷ���ʽΪ
________________________��
�ο��𰸣���1���ǻ���̼̼˫�����Ȼ����ڢۢ�
��2������
��3��Cl2+2Br-==Br2+2Cl-
���������
�����Ѷȣ�һ��