1、填空题 空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下
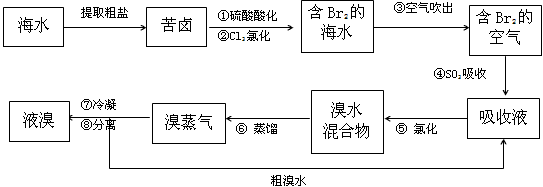
(1)溴在周期表中位于______周期,______族。
(2)步骤④的离子方程式:______________________________。
(3)已知溴的沸点是58.5℃,步骤⑥的蒸馏过程中,溴出口温度为何要控制在80-90℃。温度过高或过低都不利于生产____________,请解释原因:________________________。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是____________,分离时液溴从分离器的_________(填“上口”或“下口”)排出。
(5)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”:________________________________________________。
2、选择题 关于海洋与化学的下列说法不正确的是( )
A.海水中所含有的元素大部分以盐的形式存在
B.海水经过加碱、加酸后,浓缩、过滤、干燥、电解制得金属镁
C.元素周期表中列出的元素目前有80多种能在海水中找到
D.海水中的常量元素具有开发的价值而微量元素不具有开发的价值
3、填空题 目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下
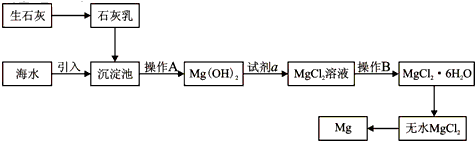
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是_______________________,写出在沉淀池的离子方程式_____________________。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的_________________。
(3)操作A是_______________, 操作B是__________________。
(4)加入的足量试剂a是__________________(填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为___________________。从考虑成本和废物循环利用的角度,副产物氯气可以用于_________________。
(6)海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
_________________________。
(7)有同学认为:可直接加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你______________(填“同意”或“不同意”)该同学的想法,理由是
_______________________。
4、选择题 海洋具有十分巨大的开发潜力。只通过物理变化就能从海水中提取的物质是
[? ]
A.碘单质
B.烧碱
C.淡水
D.氯气
5、选择题 不需要化学变化就能够从海水中获得的物质是
[? ]
A.氯.溴.碘
B.钠.镁.铝
C.烧碱.氢气
D.氯化钠