1、填空题 某温度时,在1.0 L密闭容器内加入2.0 mol SO2和1.2 mol O2,发生反应: 2SO2(g)+O2(g) 2SO3 (g) 请回答:
2SO3 (g) 请回答:
(1)反应进行2 min后,测得SO2为1.4 mol,则2 min内v(SO3)=____mol/(L.min)。
(2)若升高温度能使化学平衡向逆反应方向移动,则正反应是____(填“放热”或“吸 热”)反应。
(3)反应进行8 min后达平衡,测得c(SO3) =8c(O2),则SO2的平衡转化率是____。
(4)该温度下,此反应的平衡常数K的数值是____。
参考答案:
(1)0.30
(2)放热
(3)96%(或0. 96)
?(4)2400
本题解析:
本题难度:一般
2、选择题 对于可逆反应2AB3(g)?A2(g)+3B2(g),正反应吸热,下列图象正确的是( )
A.
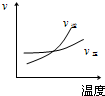
B.
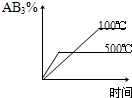
C.
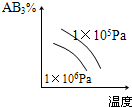
D.
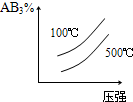
参考答案:BD
本题解析:
本题难度:一般
3、填空题 高炉炼铁中发生的基本反应之一是:FeO(s)+CO(g) Fe(s)+CO2(g),其△H>0,其平衡常数可表达为
Fe(s)+CO2(g),其△H>0,其平衡常数可表达为
Kc=[CO2]/[CO],已知1100℃时,Kc=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比______,平衡常数Kc_______
(本小题空格均备选“增大”、“减小”或“不变”)。
(2)1100℃时测得高炉中[CO2]=0.025mol・L-1,[CO]=0.1mol・L-1,在这种情况下,该反应是否处于平衡状态________(填“是”或“否”),此时,化学反应速率V(正)________V(逆)(填“大于”、“小于”或“等于”),其原因是__________________。
参考答案:(1)增大;增大
(2)否;大于;此时[CO2]/[CO]<0.263,因温度不变,K值不变,为增大[CO2]/[CO]比值,需V(正)>V(逆)
本题解析:
本题难度:一般
4、填空题 如图所示是800℃时,X、Y、Z三种气体的浓度(c)随时间(t)的变化情况,t2是反应达到平衡的时间,写出反应的化学方程式:______.
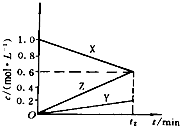
参考答案:由图象可以看出,反应中X的物质的量减少,应为反应物,Y、Z的物质的量增多,应为生成物,
当反应进行到2min时,△n(X)=0.4mol,△n(Y)=0.2mol,△n(Z)=0.6mol,
则△n(X):△n(Y):△n(Z)=2:1:3,参加反应的物质的物质的量之比等于化学计量数之比,
则反应的方程式为:2X Y+3Z,故答案为:2X
Y+3Z,故答案为:2X Y+3Z.
Y+3Z.
本题解析:
本题难度:简单
5、选择题 汽车上的催化转化器,可将尾气中的主要污染物转化成无毒物质,反应为:
 在某温度时.,用气体传感器测得不同时间的NO和CO浓度如表
在某温度时.,用气体传感器测得不同时间的NO和CO浓度如表
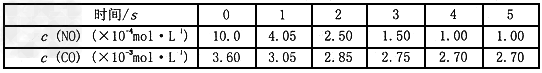
经分析,得出结论不正确的是
[? ]
A. 该反应转化较快,具有存实际意义
B. 催化转化器在冬季时对废气转化效率比夏季更高
C. 2s末的平均反应速率 ?
?
D. 在该温度下,反应的平衡常数K=5000
参考答案:C
本题解析:
本题难度:一般