1、选择题 将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为CO2+2Mg  C+2MgO,该反应属于:
C+2MgO,该反应属于:
[? ]
①化合反应 ②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥离子反应 ⑦非氧化还原反应
A.①③⑦
B.②③⑥
C.③⑤
D.④⑥
参考答案:C
本题解析:
本题难度:简单
2、填空题 (12分)已知溶液中:还 原性HSO3->I-,氧化性IO3-> I2 > SO42-。
原性HSO3->I-,氧化性IO3-> I2 > SO42-。
在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
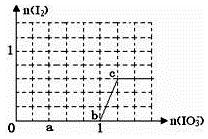
(1)写出a点反应的离子方程式_____________________;
反应中还原剂是_________;被还原的元素是_________。
(2)写出b点到c点反应的离子方程式________________。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为______mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为_______________________。
参考答案:(12分) (1) ?3HSO32-_+IO3-_==3SO42-+I-+3H+_;__NaHSO3___;__碘元素___。
(2) _____5I-+ IO3-_+6H+==3I2+3H2O____。
(3) __0.4或1.12__mol 。(4) __2 IO3-_+5 HSO32-_==I2+5SO42-+3H++H2O_
本题解析:略
本题难度:一般
3、填空题 (8分)铜在常温下能被稀HNO3溶解:3Cu+8HNO3(稀)="=" 3Cu(NO3)2+2NO↑+4H2O
⑴ 请将上述反应改写成离子方程式:_____________________。
⑵ 上述反应中氧化剂是?,没有参加氧化还原反应的硝酸占总硝酸的比例_____。
(3)取1.92gCu与一定量浓HNO3恰好完全反应,生成气体颜色由红棕色逐渐变成无色,共得到标准状况下气体1.12L,则参加反应的硝酸为_____________mol。
参考答案:⑴ 3Cu+8H++2NO3-==3Cu2++2NO↑+4H2O? ⑵? HNO3? 3/4?(3)0.11
本题解析:(1)考查离子方程式的书写。在改写离子方程式时,关键是找准哪些物质可以用离子符合来表示,哪些可以用化学式来表示。只有既能溶于水,又能完全电离的物质才能用离子来表示,其他的均用化学式表示。
(2)由方程式可知8mol硝酸参加反应其中只有2mol硝酸被还要,其氮元素的化合价由+5价降低到+2价,所以没有参加氧化还原反应的硝酸占总硝酸的比例3/4。
(3)生成气体颜色由红棕色逐渐变成无色,说明气体是NO和NO2的混合气体,其物质的量是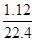 =0.05mol,根据氮元素守恒可知被还原的硝酸的物质的量就是0.05mol。1.92gCu被氧化生成Cu(NO3)2,其物质的量是
=0.05mol,根据氮元素守恒可知被还原的硝酸的物质的量就是0.05mol。1.92gCu被氧化生成Cu(NO3)2,其物质的量是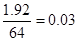 mol。同样根据氮元素守恒可知没有被还原的硝酸的物质的量就是0.03mol×2=0.06mol,参加反应的硝酸为0.06mol+0.05mol=0.11mol。
mol。同样根据氮元素守恒可知没有被还原的硝酸的物质的量就是0.03mol×2=0.06mol,参加反应的硝酸为0.06mol+0.05mol=0.11mol。
本题难度:一般
4、填空题 已知常温常压下:① 3Cl2+2NH3→N2+6HCl?,②3Cl2+8NH3→N2+6NH4Cl?
(1)完成并配平反应③的化学方程式,并标出电子转移方向和数目:
③ 3Cl2+4NH3→ ?
(2)在反应③中:还原剂是?,还原产物是?。
(3)若按③反应后产生气体4.48 L(标准状况),则被氧化的气体的物质的量是?mol。
参考答案:
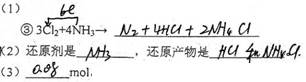
本题解析:略
本题难度:一般
5、选择题 用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S
下列说法正确的是(? )
A.反应中硫元素被氧化,所有铁元素均被还原
B.还原剂是S2-和Cu+,氧化剂是Fe3+
C.氧化产物是S,还原产物是Cu2+和Fe2+
D.当转移1 mol e-时,有46 g CuFeS2参加反应
参考答案:D
本题解析:A项CuFeS2中铁元素的化合价为+2价,反应物Fe3+的化合价为+3价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,错误;B项CuFeS2中Cu为+2价、Fe为+2价,S为-2价,只有S元素的化合价只有降低,氧化产物是S,还原产物是Fe2+,所以B、C均错误;D项CuFeS2+4Fe3+=Cu2++5Fe2++2S中1mol CuFeS2参与反应,转移4mol电子,则转移1 mol e-时,CuFeS2为0.25mol,质量是46g,故D正确。
点评:本题涉及的反应比较复杂,主要是CuFeS2中物质化合价的分析是难点,本题属于较难题。
本题难度:一般