1������� ��ҩ���й��ġ��Ĵ�����֮һ����Զֵ�������セ����Ҳ��Զ�ἤ��������ȥ�ܷ�ͼǿ���ڻ�ҩ�ڷ�����ըʱ���������µķ�Ӧ��2KNO3+C��S===K2S+2NO2��+CO2�������б�������Ԫ����?����������??�� ??
�ο��𰸣���3�֣� ̼��? KNO3����?��1��
����������ؼ�����ʽ��֪��������е�Ԫ�صĻ��ϼ۴ӣ�5�۽��͵���4�ۣ��õ�1�����ӡ�̼Ԫ�صĻ��ϼ۴�0�����ߵ���4�ۣ�ʧȥ4�����ӣ�SԪ�صĻ��ϼ۴�0�۽��͵���2�ۣ��õ�2�����ӣ����Ա�������Ԫ����̼��������������غ�S��
�����������ǻ���������Ŀ��飬������ؿ���ѧ���Ļ���֪ʶ���ѶȲ�����Ĺؼ���ȷ����й�Ԫ�صĻ��ϼۣ�Ȼ����������������ü��ɡ�
�����Ѷȣ�һ��
2������� ��1�����Ϸ�����(��Ҫ�ɷ�V2O5)��ϡ���ᡢ���������Һ��ϣ���ַ�Ӧ��������Һ�����ԣ���VO2����K����SO42-�ȡ�д���÷�Ӧ�Ļ�ѧ����ʽ_________________________________��
��2��������������Һ�м���KClO3��Һ����ַ�Ӧ����Һ����������VO2+��Cl����д������ƽ�÷�Ӧ�����ӷ���ʽ�����������ת�Ƶ���Ŀ�ͷ���______________________��
��3����20.00 mL��0.1 mol��L��1 VO2+��Һ�У�����0.195 gп�ۣ�ǡ����ɷ�Ӧ����ԭ���������______________________________________________________________��
a��V? b��V2��? c��VO2+? d��VO2��
��4����֪V2O5�ܺ����ᷴӦ����������VO2��������дһ�����ӷ�Ӧ����ʽ��˵����ԭ�ԣ�SO32-��Cl����VO2��__________________________________��
�ο��𰸣���1��V2O5��K2SO3��2H2SO4=2VOSO4��K2SO4��2H2O
��2��ClO3-��6V6e��O2����3H2O=Cl����6VO2+��6H��
��3��b
��4��Cl2��SO32-��H2O=2Cl����2H����SO42-
�����������1��K2SO3Ϊ��ԭ������������ΪK2SO4��V2O5Ϊ����������ԭ����ΪVO2����
��2��KClO3��VO2��������VO2+��������ԭ��Cl�������ӷ���ʽΪClO3-��6VO2����3H2O=
Cl����6VO2+��6H����ת��6 mol e����
��3�����ݵ��ӵ�ʧ�غ�ã�
 ��2��0.02 mol��0.1 mol��L��1��(5��x)
��2��0.02 mol��0.1 mol��L��1��(5��x)
x��2��b��ȷ��
��4������֪�ã�Cl����VO2��������Cl2��SO32-��H2O=2Cl����2H����SO42-
���Ƴ���ԭ��SO32-��Cl����
�����Ѷȣ�һ��
3������� ��֪��ӡ������ʱ�ײ�������������Ũ�ȹ���ʱ�������к�����������ǿ�����ԣ�����ʹʪ��ĵ⻯�ص�����ֽ���������г�������ת��Ϊ������
(1)д������ƽ������Ӧ�����ӷ���ʽ________.?
(2)�÷�Ӧ����������________����ԭ������________________��
(3)�÷�Ӧ�������ַ�Ӧ����������ӦΪ________ת��Ϊ________���ڻ�ԭ��Ӧ���̵ķ�ӦʽΪ________��
(4)��Ӧ��1?mol����________(��õ�����ʧȥ��)________mol���ӣ�
�ο��𰸣�(1)O3��2I����H2O===2OH����I2��O2
(2)O3����OH��(��KOH)
(3)��I������I2��
��O3��H2O��2e��===2OH����O2
(4)�õ�����2
���������
�����Ѷȣ�һ��
4������� ���ݷ�Ӧ3Cu+8HNO3=3Cu(NO3)2+2NO��+4H2O?�ش��������⣺
��1����������?������������?��
��2����������������������ʵ�������?��
��3������2 mol HNO3����ԭʱ�������������ʵ�����Ϊ?����Ӧ��ת�Ƶĵ�����Ϊ?;
��4��������6�����ʣ�K2SO4��K2SO3��I2��H2SO4��KIO3��H2O���һ��������ԭ��Ӧ����֪�ڷ�Ӧ��K2SO3ʧȥ���ӡ���ش��������⣺
����6�����ʷֱ����������Ӧ�ĺ����ϣ����һ����ѧ����ʽ��������ƽ����
________��________��________ �� ________��________��________
�ο��𰸣���1��HNO3?Cu(NO3)3?��2��2��3?��3��192g? 6NA��3.612��1024
��4��K2SO3 + KIO3 + H2SO4 ��I2 + K2SO4 + H2O
����������ڷ�Ӧ��ͭ�Ļ��ϼ���0��+2�ۣ�������������ԭ��������������Cu(NO3)3��HNO3�е��Ļ��ϼ���+5��+2�ۣ�����ԭ���������������ɻ�ԭ����N0���ڷ�Ӧ��8?mol HNO3��Ӧ��ֻ��2mol HNO3����������������Ϊ3mol��64g�Mmol=192g.��������������������ʵ�����,2:3.ת��ת�Ƶĵ�����Ϊ��3��2�Σ�=6NA=3.612��1024���ڷ�Ӧ��K2SO3ʧȥ���ӣ�˵�����ǻ�ԭ������������K2SO4��������������ǿ�����Կ������������ĵ���KIO3��KIO3�����������±������������ɵĻ�ԭ����I2�����ݻ�ѧ��Ӧ�Ĺ��̾���ԭ��������ϵĹ��̿�֪���⼸��������ϵķ�ӦΪK2SO3 + KIO3 + H2SO4 ��I2 + K2SO4 + H2O��
�����Ѷȣ�һ��
5�������� ��8�֣�����Cu+2H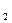 SO
SO ��Ũ��
��Ũ�� CuSO
CuSO +SO
+SO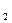 ��+2H
��+2H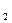 O����������⣨��֪Cu�����ԭ������Ϊ64����
O����������⣨��֪Cu�����ԭ������Ϊ64����
��1���÷�Ӧ����������____________����������Ԫ����______________��
��2������32 g Cu �ܽ�ʱ������ԭ��H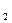 SO
SO ������Ϊ___________g��
������Ϊ___________g��
�ο��𰸣���1��H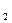 SO
SO Cu
Cu
��2��49
���������CuԪ�ػ��ϼ����ߣ�H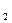 SO
SO ��SԪ�ػ��ϼ۽��ͣ���˿ɻش�1�����˷�Ӧ�У�ÿ2��H
��SԪ�ػ��ϼ۽��ͣ���˿ɻش�1�����˷�Ӧ�У�ÿ2��H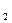 SO
SO ���Ӳ��뷴Ӧ��ֻ��1��H
���Ӳ��뷴Ӧ��ֻ��1��H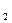 SO
SO ���ӱ���ԭ����64 g Cu �ܽ�ʱ��ֻ��98 g H
���ӱ���ԭ����64 g Cu �ܽ�ʱ��ֻ��98 g H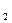 SO
SO ?����ԭ��
?����ԭ��
�����Ѷȣ�һ��