微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 镁、铝、铜组成的混合物10.3克,在空气中充分加热至恒重,质量变为13.5克.如果将所得固体溶解,需要消耗6mol?L-1的硫酸
A.0.1mol
B.0.2mol
C.50mL
D.60mL
选择题 镁、铝、铜组成的混合物10.3克,在空气中充分加热至恒重,质量变为13.5克.如果将所得固体溶解,需要消耗6mol?L-1的硫酸
A.0.1mol
B.0.2mol
C.50mL
D.60mL
本题答案:B
本题解析:分析:镁、铝、铜组成的混合物在空气中充分加热至恒重,生成金属氧化物,固体增加的质量3.2g是氧元素的质量,金属氧化物与硫酸反应生成硫酸盐与水,水中氧原子来源于金属氧化物,水中氢原子来源于硫酸,利用氧原子计算生成的水的物质的量,根据水计算参加反应的硫酸的物质的量,据此计算消耗硫酸溶液体积.
解答:镁、铝、铜组成的混合物在空气中充分加热至恒重,生成金属氧化物,固体增加的质量13.5g-10.3g=3.2g是氧元素的质量,所以氧原子的物质的量为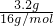 =0.2mol.
=0.2mol.
金属氧化物与硫酸反应生成硫酸盐与水,水中氧原子来源于金属 91eXaM.org氧化物,根据氧原子守恒,生成水的物质的量为0.2mol.
水中氢原子来源于硫酸,根据氢原子守恒可知,参加反应硫酸的物质的量为0.2mol.
所以需要消耗6mol?L-1的硫酸的体积为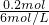 =0.033L=33ml.
=0.033L=33ml.
故选:B.
点评:考查混合物的有关计算,难度中等,关键判断固体增加的质量是氧元素的质量及根据守恒计算,用常规方法无法计算.是对学生综合能力的考查.
本题所属考点:【金属及其化合物】
本题难易程度:【困难】
Water is a boon in the desert,but the drowning man curses it. 水是沙漠里的恩物,快淹死的人却诅咒它。