微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下列叙述中正确的是
A.标准状况下,22.4LH2SO4中含有6.02×1023个硫原子
B.常温常压下,O2和O3的混合物16g中含有6.02×1023 91exam .org个氧原子
C.500mL0.5mol?L-1的Fe2(SO4)3溶液中SO42-浓度为0.75mol?L-1
D.0.5molOH-中含有3.01×1023个电子
选择题 下列叙述中正确的是
A.标准状况下,22.4LH2SO4中含有6.02×1023个硫原子
B.常温常压下,O2和O3的混合物16g中含有6.02×1023个氧原子
C.500mL0.5mol?L-1的Fe2(SO4)3溶液中SO42-浓度为0.75mol?L-1
D.0.5molOH-中含有3.01×1023个电子
本题答案:B
本题解析:分析:A、根据气体摩尔体积的使用范围判断;
B、它们是同素异形体,根据质量、摩尔质量、原子数、阿伏加德罗常数之间的关系计算;
C、根据同一溶质中,溶质的浓度与不发生水解的离子浓度之比等于其系数之比;
D、根据物质的量、离子数、电子数、阿伏加德罗常数之间的关系计算判断;
解答:A:H2SO4不是气体,不能使用气体摩尔体积22.4L/mol,所以22.4LH2SO4的物质的量不是1mol,故A错误;
B:O2和O3是同素异形体,分子都是由氧原子构成,O2和O3的混合物只含有氧原子,氧原子的摩尔质量是16g/mol,
所以,16gO2和O3的混合物含有氧原子数为N=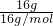 ×6.02×1023mol-1=6.02×1023,故B正确;
×6.02×1023mol-1=6.02×1023,故B正确;
C:根据Fe2(SO4)3组成可知,SO42-浓度是Fe2(SO4)3浓度的3倍,所以SO42-浓度为1.5mol?L-1,故C错误;
D:一个OH-含有10个电子,0.5mol OH-中含有3.01×1023个OH-,电子数为N=0.5mol×10×6.02×1023mol-1=3.01×1024,故D错误.
故选B.
点评:阿伏加德罗常数有关的计算,题目在注重对计算关系的考查的同时,又隐含对物质状态、物质结构、氧化还原反应、电离、水解知识的考查.
本题所属考点:【化学实验】
本题难易程度:【简单】
Without respect, love cannot go far. 没有尊重的爱难以久存.