微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)已知合成氨的反应为3H2(g)+N2(g) 2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。
2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。
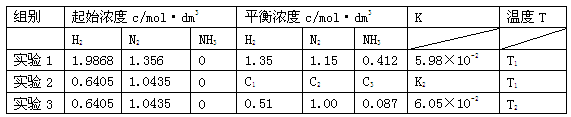
(1)下列说法可以说明合成氨反应达到平衡的是
A.恒容时,整个容器内密度不变
B.恒压时,容器内平均相对分子质量不变
C.1 mol N≡N键断裂的同时,有3mol H-H键断裂
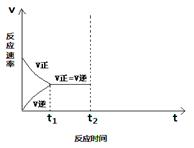
(2)当升高温度时,平衡向 方向移动(填“正”或“逆”),请画出在t2时刻升温后的v-t图,并作出必要的标注。
(3)表中实验2的K2= ,温度T1、T2的大小关系是 ,你判断的理由是 。
填空题 (16分)已知合成氨的反应为3H2(g)+N2(g) 2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。
2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。

(1)下列说法可以说明合成氨反应达到平衡的是
A.恒容时,整个容器内密度不变
B.恒压时,容器内平均相对分子质量不变
C.1 mol N≡N键断裂的同时,有3mol H-H键断裂
(2)当升高温度时,平衡向 方向移动(填“正”或“逆”),请画出在t2时刻升温后的v-t图,并作出必要的标注。

(3)表中实验2的K2= ,温度T1、T2的大小关系是 ,你判断的理由是 。
本题答案:(1)B (3分)
(2)逆&#
本题解析:
试题分析:(1)A、合成氨中所有参与反应的物质均为气体,恒容时,整个容器内气体的总质量不变,体积不变,故密度始终保持不变,A错误;B、恒压时,参与反应的气体总质量不变,平均相对分子质量与气体的总物质的量成正比,当平均相对分子质量保持不变时,各参与反应的气体的物质的量瓮中捉鳖不变了,则反应达到平衡状态,B正确;C、根据反应方程式可知,不管反应有没达到平衡当1 mol N≡N键断裂的同时,必有3mol H-H键断裂,C错误;答案为B。(2)合成氨正反应为放热反应,当升高温度时,平衡向吸热反应的方向移动,即向平衡向逆反应方向移动,升高温度,正逆反应速率都增大,但逆反应速率增大的倍数更多,随着反应的进行,逆反应速率逐渐减小,正反应速率逐渐增大,最后正逆反应速率又相等,重新建立新的平衡,且反应速率比原平衡的速率大。故图表可以表示为:

(3)① 平衡常数只与温度有关,表中实验1和实验2的温度相同,所以K相同,故K= 5.98×10-2;②利用表中实验1和实验3可知,实验3的平衡常数变大,平衡向正反应方向移动,因为该反应为放热反应,降低温度才能使平衡向正反应方向移动。
考点:考查考查化学平衡原理、化学平衡常数的应用及图表分析能力。
本题所属考点:【化学平衡】
本题难易程度:【一般】
Knowledge comes form experience alone. 知识只能来自经验.