微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)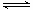 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s)
| 0
| 1
| 2
| 3
| 4
|
n(NO)(mol)
| 0.020
| 0.01
| 0.008
| 0.007
| 0.007
|
(1)写出该反应的平衡常数表达式:K= 。
已知: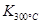 >
>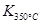 ,则该反应是 热反应。
,则该反应是 热反应。
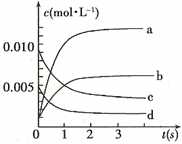
(2)图中表示NO2的变化的曲线是 ;用O2表示从0~2 s内该反应的平均速率v= ;
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正( O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
填空题 (12分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)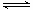 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s)
| 0
| 1
| 2
| 3
| 4
|
n(NO)(mol)
| 0.020
| 0.01
| 0.008
| 0.007
| 0.007
|
(1)写出该反应的平衡常数表达式:K= 。
已知: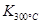 >
>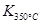 ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2的变化的曲线是 ;用O2表示从0~2 s内该反应的平均速率v= ;

(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
本题答案:(1)K=C(NO2)²/C(NO)²?
本题解析:
试题分析:(1)平衡常数表达式等于生成物的浓度幂之积比上反应物的浓度幂之积, K=C(NO2)²/C(NO)²?C(O2) 由K300℃>K350℃ 知,温度越高K越小,说明正反应是放热反应;(2)2s内用NO表示的平均反应速率v(NO)=△n/(v.△t)=(0.02-0.008)/(2*2)=3.0×10-3mol?L-1?s-1速率之比等于化学计量数之比,所以v(O2)=1/2v(NO)=1.5×10-3mol?L-1?s-1(3)a、NO2速率无论是否达到平衡都等于2倍的O2速率,错误;b、此反应化学计量数前后不相等,所以压强不变说明反应达到平衡了,正确;c、v逆(NO)=2v正(O2) 中 NO和O2速率之比等于化 学计量数之比且为正逆双向,正确;d、由于该反应体积2L不变,且均为气体,所以密度不变,不能说明达到化学平衡状态,错误。(4)a、分离出NO2气体速率减小,平衡向正反应方向移动,错误;b、升高温度反应速率增大,该反应为放热反应,平衡向左移动,错误;c、增大O2的浓度,反应速率增大,平衡向右移动,正确;d、选择高效催化剂反应速率增大,但是平衡不移动,错误。
考点:用化学平衡常数进行计算;反应速率的定量表示方法
本题所属考点:【化学平衡】
本题难易程度:【一般】
The highest towers begin from the ground. 万丈高楼平地起.