|
|
|
已知:2Zn(s)+O2(g)==="2ZnO(s)" ΔH1=-701.0 kJ・mol-1【热化学方程式】
2016-12-26 23:37:40
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 已知:2Zn(s)+O2(g)==="2ZnO(s)" ΔH1=-701.0 kJ・mol-1
2Hg( l)+O2(g)==="2HgO(s)" ΔH2=-181.6 kJ・mol-1
则反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH为
| A.+519.4 kJ・mol-1 | B.+259.7 kJ・mol-1
| | C.-259.7 kJ・mol-1 | D.-519.4 kJ・mol-1
|
选择题 已知:2Zn(s)+O2(g)==="2ZnO(s)" ΔH1=-701.0 kJ・mol-1
2Hg(l)+O2(g)==="2HgO(s)" ΔH2=-181.6 kJ・mol-1
则反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH为
| A.+519.4 kJ・mol-1 | B.+259.7 kJ・mol-1
|
| C.-259.7 kJ・mol-1 | D.-519.4 kJ・mol-1
|
本题答案:C
本题解析:
试题分析:根据盖斯定律可知:Zn(s)+HgO(s)===ZnO(s)+Hg(l) ΔH=1/2ΔH1-1/2ΔH2=

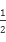
×(-701.0 kJ・mol-1)-
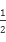
×(-181.6 kJ・mol-1)=-259.7 kJ・mol-1,故本题选C。
考点:盖斯定律应用计算。
本题所属考点:【热化学方程式】
本题难易程度:【一般】
Life is too short to waste. 生命短促,不容浪费.

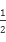 ×(-701.0 kJ・mol-1)-
×(-701.0 kJ・mol-1)-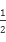 ×(-181.6 kJ・mol-1)=-259.7 kJ・mol-1,故本题选C。
×(-181.6 kJ・mol-1)=-259.7 kJ・mol-1,故本题选C。