微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (11分)应用化学学科知识,回答下列问题
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。已知在常温常压下:
2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) △H = -1275.6 kJ/mol
2CO(g)+O2(g)=2CO2(g) △H = -566.0 kJ/mol
H2O(g)=H2O(1) △H = -44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ________。
(2)水煤气经压缩升温后进入10m3甲醇合成塔,在催化剂 作用下,进行甲醇合成,主要反应是:2H2(g) + CO(g)  CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
物质
| H2
| CO
| CH3OH
|
浓度/(mol・L-1)
| 0.2
| 0.1
| 0.4
|
比较此时正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”)。
(3)已知A和B在一定条件下可建立如下平衡:2A(g)+B(g)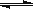 2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
①达到平衡所需时间是Ⅰ Ⅱ(填“>”、“<”或“=”,下同)。达到平衡后,两容器中C的体积分数关系是Ⅰ Ⅱ。
②平衡时,测得容器Ⅱ中的压强减小了30%,则该容器中A的转化率为 。
填空题 (11分)应用化学学科知识,回答下列问题
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。已知在常温常压下:
2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) △H = -1275.6 kJ/mol
2CO(g)+O2(g)=2CO2(g) △H = -566.0 kJ/mol
H2O(g)=H2O(1) △H = -44.0 kJ/mol
来源:91考试网 www.91exAm.org则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ________。
(2)水煤气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g) + CO(g)  CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
物质
| H2
| CO
| CH3OH
|
浓度/(mol・L-1)
| 0.2
| 0.1
| 0.4
|
比较此时正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”)。
(3)已知A和B在一定条件下可建立如下平衡:2A(g)+B(g)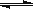 2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
①达到平衡所需时间是Ⅰ Ⅱ(填“>”、“<”或“=”,下同)。达到平衡后,两容器中C的体积分数关系是Ⅰ Ⅱ。
②平衡时,测得容器Ⅱ中的压强减小了30%,则该容器中A的转化率为 。
本题答案:(1)CH3OH(l)+O2(g)=CO(g)+2H2O(l
本题解析:
试题分析:(1)根据盖斯定律,将已知反应(①-②+③×4)÷2得到CH3OH(l)+O2(g)=CO(g)+2H2O(l),所以该反应的△H=[(-1275.6kJ/mol)-(-566.0kJ/mol)-(-44.0kJ/mol)×4]÷2=442.8kJ?mol-1,即CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ?mol-1。
(2)由表中数据可知,平衡时时氢气的浓度为0.2mol/L、CO的浓度为0.1mol/L、甲醇的浓度为0.4mol/L,则此时的浓度商Qc= =100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆。
=100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆。
(3)①平衡:2A(g)+B(g) 2C(g),是一个反应后气体系数和减小的反应,所以恒容容器下,反应达到平衡状态,恒压容器中随反应进行,为保持恒压,压强增大,达到平衡所需时间少,平衡正向移动,CO2的体积分数增大,CO2的体积分数关系是,恒压容器I大于恒容容器。
2C(g),是一个反应后气体系数和减小的反应,所以恒容容器下,反应达到平衡状态,恒压容器中随反应进行,为保持恒压,压强增大,达到平衡所需时间少,平衡正向移动,CO2的体积分数增大,CO2的体积分数关系是,恒压容器I大于恒容容器。
②在500℃时,分别将2mol A和1mol B置于恒容容器Ⅱ中(两容器起始容积都为10L),设A消耗物质的量为x 2A(g)+B(g) 2C(g)
2C(g)
起始量(mol) 2 1 0
变化量(mol) x 0.5 x x
平衡量(mol) 2-x 1-0.5x x
容器Ⅱ中的压强减小了30%,气体物质的量减小30%
3-3×30%=2-x+1-0.5x+x
X=1.8mol
A的转化率=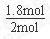 ×100%=90%。
×100%=90%。
考点:考查盖斯定律的应用、化学平衡计算以及外界条件对平衡状态的影响等
本题所属考点:【热化学方程式】
本题难易程度:【困难】
He who mistrusts most should be trusted least. 最不信任别人的人最不应该得到信任.