微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1
Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1
则反应Fe2O3(s)+CO(g)=2FeO(s)+CO2(g)的△H=__________;
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解).写出电解总反应离子方程式____________________;
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的___极发生_ __反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为______,消耗硫酸的物质的量是_____________。
填空题 (12分)工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1
Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1
则反应Fe2O3(s)+CO(g)=2FeO(s)+CO2(g)的△H=__________;
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解).写出电解总反应离子方程式____________________;
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的___极发生___反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为______,消耗硫酸的物质的量是_____________。
本题答案:(1)+411.20kJ/mol (2)2Zn2+
本题解析:
试题分析:(1)已知热化学方程式①Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1,②Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1,则根据盖斯定律可知①+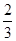 ×②得Fe2O3(s)+CO(g)=2FeO(s)+CO2(g),所以该反应的反应热△H=+411.20kJ/mol;
×②得Fe2O3(s)+CO(g)=2FeO(s)+CO2(g),所以该反应的反应热△H=+411.20kJ/mol;
(2)电解硫酸锌溶液时,阳极上氢氧根离子失去电子发生氧化反应,生成氧气。阴极上锌离子得到电子发生还原反应生成锌,电解反应的离子方程式为:2Zn2++2H2 O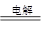 2Zn+O2↑+4H+;
2Zn+O2↑+4H+;
(3)锌、铁和电解质溶液构成的原电池中,锌的金属性强于铁,因此锌作负极,发生氧化反应;
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,氢气的物质的量是4.48L÷22.4L/mol=0.2mol,所以该反应转移的电子数=0.2×2×NA=0.4NA;氢气中氢原子来源于硫酸,根据氢原子守恒得硫酸的物质的量是0.2mol。
考点:考查反应热的计算、电化学原理的应用
本题所属考点:【热化学方程式】
本题难易程度:【一般】
Cloudy mornings turn to clear evenings. 早见云雾晚见晴。