|
|
|
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是 ①【化学反应与能量】
2016-12-27 09:41:12
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下列各组热化学方程式中,化学反应的ΔH前者大 于后者的是
①C(s)+O2(g)===CO2(g)ΔH1 C(s)+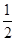 O2(g)===CO(g)ΔH2 O2(g)===CO(g)ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+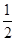 O2(g)===H2O(l)ΔH5 2H2(g)+O2(g)===2H2O(l)ΔH6 O2(g)===H2O(l)ΔH5 2H2(g)+O2(g)===2H2O(l)ΔH6
④CaCO3(s)===CaO(s)+CO2(g)ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s)ΔH8
A.①
B.④
C.②③④
D.①②③
|
选择题 下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①C(s)+O2(g)===CO2(g)ΔH1 C(s)+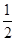 O2(g)===CO(g)ΔH2 O2(g)===CO(g)ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+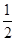 O2(g)===H2O(l )ΔH5 2H2(g)+O2(g)===2H2O(l)ΔH6 O2(g)===H2O(l )ΔH5 2H2(g)+O2(g)===2H2O(l)ΔH6
④CaCO3(s)===CaO(s)+CO2(g)ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s)ΔH8
A.①
B.④
C.②③④
D.①②③
|
本题答案:C
本题解析:
试题解析:①都为放热反应,△H<0,前者完全反应,放出的热量多,则△H1<△H2,故①错误;②都为放热反应,△H<0,由于S(s)→S(g)吸热,则前者放出的热量少,则△H3>△H4,故②正确;③都为放热反应,△H<0,消耗的氢气越多,则放出的热量越多,则△H5>△H6,故③正确;④前者为吸热反应,△H7>0,后者为放热反应,△H8<0,则△H7>△H8,故④正确.故选C.
考点:反应热的大小比较
本题所属考点:【化学反应与能量】
本题难易程度:【一般】
Cheerfulness is health; its opposite, melancholy, is disease. 欢乐就是健康,忧郁就是病痛。