|
|
|
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO32-。向【有关氧化还原反应的计算】
2016-12-27 13:27:15
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是
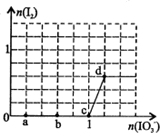
A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3来源:91考试网 91exam.org-+ 2IO3- =I2+5SO42-+3H++H2O
|
选择题 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是

A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3-+ 2IO3- =I2+5SO42-+3H++H2O
|
本题答案:D
本题解析:
试题分析:向NaHSO3的溶液中加入IO3-溶液,开始没有产生I2,在a点首先碘发生反应:6HSO3-+2IO3- = 6SO42-+2I-+6H+。在该反应中还原剂是NaHSO3,其中被氧化的元素是S元素,错误;B.由于在b点时n(IO3-)=0.6mol,反应消耗HSO3-的物质的量是1.8mol,发生的反应是:6HSO3-+2IO3- = 6SO42-+2I-+6H+。错误;C.c点到d点由于反应产生I
来源:91考试网 91ExaM.org2,所以发生的反应是:5I-+IO3- +6H+=3I2+3H2O,根据图像可知产生I2的物质的量是0.6mol。由于发生反应每转移5mol的电子,产生3mol的I2。现在产生0.6mol的I2,所以一共转移1mol电子,错误;D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,由于开始时KIO3过量,所以发生反应6HSO3-+2IO3- = 6SO42-+2I-+6H+产生的I-立即被氧化变为I2,因此开始时总反应的离子方程式是:5HSO3-+ 2IO3- =I2+5SO42-+3H++H2O,正确。
考点:考查氧化还原反应中电子转移、反应的先后顺序及反应产物的判断的知识。
本题所属考点:【有关氧化还原反应的计算】
本题难易程度:【一般】
A good name is better than riches. 美名胜过金钱。