| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
(10分)湿法炼锌为现代炼锌的主要方法,下列是以硫化锌精矿为原【未知】
④用Ag2SO4除去Cl一,发生的反应为Ag2SO4+2Cl一  2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。 2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。(3)控制一定条件,用惰性电极电解硫酸锌溶液制取锌,锌在____极析出,阳极反应式为__________。 填空题 (10分)湿法炼锌为现代炼锌的主要方法,下列是以硫化锌精矿为原料制备单质锌的工业流程。 |
 2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。
2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。 2AgCl+ SO42-可知室温下该反应的平衡常数
2AgCl+ SO42-可知室温下该反应的平衡常数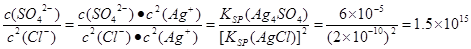 。
。本题所属考点:【未知】
本题难易程度:【困难】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:(本题共13分)A、B、C、D、E五种.. | ||