微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1mol Fe粉与1mol水蒸气充分反应转移的电子数为3NA
B.电解精炼铜时,若转移了NA 个电子,则阴极析出32 g铜
C.6.8克熔融的KHSO4混中含有0.1NA个阳离子
D.标准状况下,11.2L四氯化碳所含分子数为0.5NA
选择题 NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1mol Fe粉与1mol水蒸气充分反应转移的电子数为3NA
B.电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜
C.6.8克熔融的KHSO4混中含有0.1NA个阳离子
D.标准状况下,11.2L四氯化碳所含分子数为0.5NA
本题答案:B
本题解析:
试题分析:Fe粉与水蒸气反应的化学方程式为:3Fe +4H2O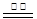 Fe3O4 +4H2,可知铁粉过量,1mol水蒸气反应转移的电子为2mol,故转移的电子为2NA,A错;电解精炼铜时,在阴极是C u2+放电,当转移了NA个电子时,有0.5mol的Cu2+放电,则阴极析出32 g铜,B对;6.8克的KHSO4的物质的量为0.05moi,在熔融状态下HSO4―不能电离出H+,所以阳离子只有0.05mol的K+,个数为0.05NA,C错;标准状况下四氯化碳是液体,知道体积不能有气体的摩尔体积计算物质的量,故无法计算分子个数,D错。
Fe3O4 +4H2,可知铁粉过量,1mol水蒸气反应转移的电子为2mol,故转移的电子为2NA,A错;电解精炼铜时,在阴极是C u2+放电,当转移了NA个电子时,有0.5mol的Cu2+放电,则阴极析出32 g铜,B对;6.8克的KHSO4的物质的量为0.05moi,在熔融状态下HSO4―不能电离出H+,所以阳离子只有0.05mol的K+,个数为0.05NA,C错;标准状况下四氯化碳是液体,知道体积不能有气体的摩尔体积计算物质的量,故无法计算分子个数,D错。
考点:阿伏伽德罗常数的应用。
本题所属考点:【物质的量】
本题难易程度:【一般】
The chains of habit are too weak to be felt until they are too strong to be broken. 习惯之链很弱,往往感觉不到,一旦感觉到了,已经牢固得绷不断了。