微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (Ⅰ)(8分)某无色溶液中可 能含有Na+、SO42― 、MnO4―、 、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是??????????;肯定没有的离子是????????????。
⑵写出步骤②中的离子方程式?????????????????????????????????。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
①?????????????????????????????????????????②???????????????????????????????????。
简述设计实验证明:?????????????????????????????????????????????????????????????。
实验题 (Ⅰ)(8分)某无色溶液中可能含有Na+、SO42― 、MnO4―、 、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是??????????;肯定没有的离子是????????????。
⑵写出步骤②中的离子方程式?????????????????????????????????。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
①?????????????????????????????????????????②???????????????????????????????????。
简述设计实验证明:???????????????????????? ?????????????????????????????????????。
本题答案:(Ⅰ).(8分)⑴Na+ ?、Br―、中可能含有Na+(肯定有,因为只有它一种阳离子)、SO42― 、MnO4―肯定没有MnO4―(紫色)、<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) 、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
、Cl― 、Br―、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;说明溶液呈现碱性,所以在碱性环境中不能大量共存的离子不能存在,此处不能排除任何离子;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;说明一定有Br―离子,因为溴单质溶于四氯化碳后是橙红色的;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。判断不出是不是有氯离子,因为前面加的是氯水,其中含有氯离子,对实验是有干扰的。只能说可能有氯离子。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。肯定有亚硫酸根,溶液中的硝酸根和氢离子把它氧化成了硫酸根了,所以一定有亚硫酸根。所以溶液中肯定含有的离子是Na+ ?、Br―、
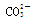 ;肯定没有的离子是MnO4―?;步骤②中的离子方程式是Cl2+2Br―== Br2+2 Cl―;
;肯定没有的离子是MnO4―?;步骤②中的离子方程式是Cl2+2Br―== Br2+2 Cl―; +Cl2+H2O ==2H++2Cl―+SO42―;SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
+Cl2+H2O ==2H++2Cl―+SO42―;SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
SO2或SO2与水作用的产物漂白了红色的溶液;SO2与NaOH反应降低了溶液的PH;
设计实验证明的方法:方案一、取上述褪色后的溶液于试管,加入NaOH溶液,溶液恢复红色,则假设二成立;
方案二、取上述褪色后的溶液于试管,用酒精灯加热,溶液恢复红色,,则假设一成立。
点评:离子推断题解法归纳:这些推断题的解法在于掌握离子的特有反应以及离子间的共存情况。在解题之前,应对所提供的离子在溶液中能否大量共存进行分析,做到心中有数。一般来说,离子间能生成沉淀、或气体、或弱电解质,以及能发生氧化还原反应的,就不能在溶液中大量共存。例如,H+与OH-?,H+与弱酸根阴离子,OH-?与弱碱阳离子,Ag+与Cl-?、Br-?、I-?、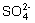 、
、 ,Ba2+、Ca2+与
,Ba2+、Ca2+与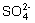 、
、 ,Fe2+与
,Fe2+与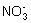 (酸性条件下),Fe3+与S2-?,Al3+与
(酸性条件下),Fe3+与S2-?,Al3+与 、S2-?等等,都不能在溶液中共存。
、S2-?等等,都不能在溶液中共存。
在具体推断过程中,要注意以下几点:
(1)?把推断离子的肯定与否定存在结合起来考虑,不要单打一。
(2)?推断过程中,前后的结论不应该矛盾。因此,前面已下结论的离子,在后面的推断过程中可不再重叙。若在分析中发现前后结论有矛盾,则应找出错误原因。
(3)?在作推断结果时,应该考虑三个方面,即肯定存在的离子,肯定不存在的离子,不能判定存在与否的离子。并且这三个方面的离子应是互相独立的,任何一种离子只能出现一次,不能重复出现。当然有的题目中不一定三种情况都需要回答,但分析问题时都应该考虑到。
本题所属考点:【探究性实验的设计与评价】
本题难易程度:【一般】
A bad padlock invites a picklock. 坏锁招人撬。