微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)
请写出下列反应的化学方程式。
(1)次氯酸在光照条件下不能稳定存在:??????????????。
(2)氨的实验室制法????????????????????。
(3)制备硅酸胶体???????????????????????。
(4)石墨与浓硫酸共热________________________
参考答案:(8分) (1) 2HClO 本题解析:
本题解析:
试题分析:所书写的化学方程式都源自于教材。
点评:本题考查的内容为化学反应方程式的书写,所要书写的化学方程式都是源自于教材中的,只要学生对教材的知识掌握的扎实,就不难解答本题。
本题难度:一般
2、选择题 有关氧化还原反应说法正确的是
A.置换反应一定是氧化还原反应
B.氧化剂具有氧化性、发生氧化反应
C.非金属单质在反应中只能得到电子做氧化剂
D.某元素从化合态变到游离态时,该元素一定是被还原
参考答案:A
本题解析:
试题分析:A置换反应是单质与化合物反应产生新的单质和新的化合物,有元素化合价的变化,一定是氧化还原反应。正确。B、氧化剂具有氧化性、发生还原反应。错误。 C、非金属单质在反应中既能得到电子做氧化剂,也能失去电子,作还原剂。错误。 D、某元素从化合态变到游离态时,该元素可能是被氧化,也可能是被还原。错误。
本题难度:一般
3、简答题 洋蓟素是一种新型的抗乙型肝炎和艾滋病病毒的化合物,其结构如图所示.请回答下列问题:
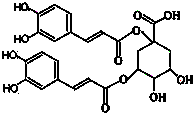
(1)洋蓟素分子中“苯环上的含氧官能团”的名称是______;它的水溶液显______(填:中、酸、碱)性.
(2)有关洋蓟素的说法错误的是______
A.是一种芳香烃
B.可以使酸性KMnO4和溴水褪色
C.能与氯化铁溶液发生显色反应
D.能发生卤代、酯化、硝化和磺化反应
E.?1mol最多可与11molNaOH反应
F.不能与新制Cu(OH)2发生变红色的反应
(3)若洋蓟素在酸性条件下水解,生成2种有机物M(含苯环)和R(不含苯环),则:
①在催化剂作用下,M与足量的H2作用下的加成产物为(写结构简式)______;
邻苯二酚与A物质发生加成反应可生成M,其化学方程式为:

则A物质的结构简式为:______;
②R的分子式为______;如果用R与浓硫酸共热,当只消去环上羧基的间位的2个官能团,并生成对称双键产物的化学反应方程式为______.
参考答案:(1)根据有机物的结构简式可知洋蓟素分子中“苯环上的含氧官能
本题解析:
本题难度:一般
4、选择题 下列反应属于氧化还原反应的是???(??)
A? CaCO3+2HCl====CaCl2+H2O+CO2↑
B? MgCl2+2NaOH====Mg(OH)2↓+2NaCl
C?CuO+H2?△?Cu+H2O
D? NaBr+AgNO3===AgBr↓+NaNO3
参考答案:C
本题解析:是否有化合价的改变是判定反应是否为氧化还原反应的标志,选项中只有C项符合题意:置换反应均为氧化还原反应,一定有化合价的升降。
本题难度:简单
5、计算题 (6分)钙元素是人体必需的常量元素,所有的细胞都需要钙元素。正常人体血液含Ca2+为2.2×10-3 ~2.7×10-3mol・L-1。现抽取某人血样10ml。稀释后用草酸铵[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙CaC2O4沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解可得到草酸(H2C2O4),并用2.0ml 5.0×10-3 mol・L-1KMnO4溶液与溶解得到的草酸恰好完全反应。据此可以求此人血液中的Ca2+的浓度,并判断其血液含钙量是否正常。(提示2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2+8H2O)
(1)配制5.0×10-3 mol・L-1KMnO4 200mL溶液,需要称取KMnO4固体的质量是 g;
(2)每消耗草酸0.5mol,转移电子的物质的量为 mol;
(3)此人血液中的Ca2+的浓度为 mol・L-1。
参考答案:(各2分)(1)0.158 (2)1&
本题解析:
试题分析:(1)n(KMnO4)= 5.0×10-3 mol・L-1×0.2L=10-3 mol,KMnO4的质量为10-3 mol×158g/mol=0.158g。(2)反应2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2+8H2O转移的电子为10e-,所以每消耗草酸0.5mol,转移电子的物质的量为1mol 。(3)根据反应方程式和元素守恒可得到关系式:2KMnO4~5H2C2O~5CaC2O4,消耗了2.0ml 5.0×10-3 mol・L-1KMnO4溶液,则CaC2O4的物质的量为:25×10-6mol,血样取了10ml,所以Ca2+的浓度为:25×10-3 mol÷(10×10-3)=2.5×10-3mol・L-1
考点:物质的量的计算、氧化还原反应的电子转移、元素守恒规律的应用。
本题难度:一般