微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在溶液中不能发生水解的离子是
A.HS-
B.CO32-
C.Fe3+
D.Br-
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列用来表示物质变化的化学反应式正确的是? [???? ]
A.碱性氢氧燃料电池的正极反应式为:?H2?+?2OH-?-?2e-=?2H2O
B.用铂电极电解硫酸铜溶液的阳极反应式为:2H2O-4e-=O2↑+?4H+
C.醋酸与稀NaOH溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l)??△H=-57.3kJ/mol
D.NaHSO3溶于水时水解的离子方程式为:HSO3-+?H2O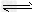 SO32-+H3O+
SO32-+H3O+
参考答案:B
本题解析:
本题难度:一般
3、选择题 25℃时,下列有关溶液中微粒的物质的量浓度关系不正确的是
A.0.1 mol・L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)
B.pH =11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)> c(OH-)>c(H+)
C.0.1 mol・L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH) =" 0.1" mol・L-1
D.0.1 mol・L-1的醋酸钠溶液20 mL与0.1 mol・L-1盐酸10 mL混合后溶液显酸性: c(CH3COO-)>c(Cl-)
>c(CH3COOH)>c(H+)
参考答案:B
本题解析:
试题分析:A.0.1 mol・L-1 (NH4)2Fe(SO4)2溶液中,由于铵根离子会发生水解反应消耗,所以c(SO42-)>c(NH4+);根据物料守恒可知:c(NH4+)>c(Fe2+);铵根离子、亚铁离子水解消耗水电离产生的OH-,破坏了水的电离平衡,最终使溶液显酸性,所以c(H+)> c(OH-);但是盐的水解程度是微弱的,盐电离产生的离子浓度大于水电离产生的离子浓度,所以c(Fe2+)>c(H+)。故溶液中离子的浓度关系是:c(SO42-)> c(NH4+) > c(Fe2+)>c(H+),正确;B.一水合氨是弱碱,当pH =11的氨水和pH=3的盐酸溶液等体积混合时,弱碱电离产生的离子恰好与盐酸中和,未电离的碱的分子会继续电离,所以溶液显碱性,c(OH-)>c(H+);c(NH4+)>c(Cl-),但是强电解质盐电离产生的离子浓度大于弱电解质一水合氨的电离,所以c(Cl-)> c(OH-),故离子浓度关系是:所得溶液中:c(NH4+)>c(Cl-)> c(OH-)>c(H+),错误;C.根据物料守恒可得在0.1 mol・L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH) =" 0.1" mol/L, 正确;D.0.1 mol・L-1的醋酸钠溶液20 mL与0.1 mol・L-1盐酸10 mL混合后所得溶液是CH3COOH和CH3COONa等物质的量的混合溶液。因为溶液显酸性:说明醋酸的电离作用大于CH3COO-水解作用,所以c(CH3COO-)>c(Cl-) >c(CH3COOH),酸的电离作用是微弱的,所以c(CH3COOH)>c(H+),因此微粒浓度关系是c(CH3COO-)>c(Cl-) >c(CH3COOH) >c(H+),正确。
考点:考查溶液中微粒的物质的量浓度关系的知识。
本题难度:一般
4、填空题 (14分)以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)?4NH3(g)+3O2(g) △H="+" 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式 .
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则 .
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N2 1mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
序号
| 第一组
| 第二组
| 第三组
| 第四组
|
t/℃
| 30
| 40
| 50
| 80
|
NH3生成量/(10
参考答案:
本题解析:
本题难度:困难
5、选择题 常温下,下列有关叙述正确的是
A.在Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.在pH=8的NaB溶液中 :c(Na+)-c(B
参考答案:
本题解析:
本题难度:一般
|