微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有三种不同浓度的稀硫酸,体积比依次3∶2∶1,它们分别与等物质的量的K2CO3、KHCO3、Al刚好完全反应,此三种硫酸的物质的量浓度比为(??? )
A.1∶1∶1
B.6∶2∶3
C.4∶3∶18
D.2∶1∶3
参考答案:C
本题解析:设三种不同浓度H2SO4(aq)的体积分别为3 L、2 L、1 L。
K2CO3+H2SO4====K2SO4+H2O+CO2↑
1 mol?? 1 mol
1 mol?? c1(H2SO4)×3 L
2KHCO3+H2SO4====K2SO4+2H2O+2CO2↑
2 mol??? 1 mol
1 mol??? c2(H2SO4)×2 L
2Al+3H2SO4====Al2(SO4)3+3H2↑
2 mol??? 3 mol
1 m
本题难度:简单
2、选择题 在10 mL 0.01 mol・L-1的纯碱溶液中,不断搅拌并逐滴加入1.2 mL 0.05 mol・L-1盐酸,完全反应后在标准状况下生成二氧化碳的体积为(???)
A.1.34 Ml
B.2.240 mL
C.0.672 mL
D.0 mL
参考答案:D
本题解析:已知n(Na2CO3)=1×10-4 mol,n(HCl)=6×10-5 mol,在纯碱溶液中逐滴加入稀盐酸,先发生反应:Na2CO3+HCl====NaCl+NaHCO3;再发生:NaHCO3+HCl====NaCl+H2O+CO2↑因为n(Na2CO3)>n(HCl),只发生第一步反应,所以没有气体放出。
本题难度:简单
3、填空题 用8g NaOH固体配制成100mL NaOH溶液,并进行有关实验,计算并回答问题
(1)配成NaOH溶液的物质的量浓度是_____;
(2)配制溶液时需要的仪器应选择___________
①? 100mL量筒?②100mL烧杯③100mL容量瓶?④胶头滴管??⑤玻棒
(3)将所得溶液与一定质量的铝充分反应,铝全部反应完,生成的气体在标准状况下体积为3.36L。铝的质量______g。
参考答案:2 mol/L?②③④⑤?? 2.7g
本题解析:略
本题难度:一般
4、选择题 设NA为阿伏加德罗常数的值,下列说法正确的是
A.一定条件下,2.3g金属钠与氧气完全反应失电子数为0.1NA
B.常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子
C.1molOH- 中含有的电子数为9NA
D.0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA
参考答案:A
本题解析:
试题分析:A、Na只有+1价,2.3g失去的电子数为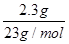 ×1NA=0.1NA;A正确;B、常温常压下,氧气和臭氧(O3)的混合物32g中含有
×1NA=0.1NA;A正确;B、常温常压下,氧气和臭氧(O3)的混合物32g中含有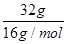 本题难度:一般
本题难度:一般
5、选择题 2.8g Fe全部溶于一定浓度、200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断正确的是
A.反应后溶液中存在Fe3+和Fe2+
B.1.12L气体是NO、NO2的混合气体
C.反应后溶液中c(NO3-)=0.85mol・L-1
D.反应后的溶液最多还能溶解1.4gFe
参考答案:C
本题解析:硝酸过量,所以不可能生成亚铜离子,选项A不正确;2.8g铁是0.05mol,失去0.15mol,如果生成的是NO,则NO是0.05mol,标准状况下的体积是1.12L。如果是NO2,则物质的量是0.15mol,所以所得气体全部是NO,选项B不正确;生成硝酸铁是0.05mol,剩余硝酸是0.02mol,所以溶液中c(NO3-)=(0.15mol+0.02mol)÷0.2L=0.85mol・L-1 ,选项C正确。0.05mol硝酸铁能溶解铁是0.025mol,质量是1.4g,但过量得硝酸还溶解铁
本题难度:一般