��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ���ǣ�������
A�������£���pHΪ1��������Һ�м���������pHΪ13������������Һǡ����ȫ�к�
B��Al3+��NO3-��Cl-��CO32-��Na+���Դ���������pH=2����Һ��
C���Ҵ������ᶼ������ˮ�����ǵ����
D���ֱ�������ʵ�����HCl��H2SO4��Ӧʱ������NaOH�����ʵ�����ͬ
�ο��𰸣�A��������к͵�ʵ��ΪH++OH-�TH2O��pHΪ1�����ᣬ
���������
�����Ѷȣ�һ��
2��ʵ���� ��ij������Һ�У����ܴ��������������ӣ�H+��K+��Ba2+��SO42����I����CO32����ȡ����Һ��������ʵ�飺
����pH��ֽ���飬����Һ��ǿ���ԣ�
��ȡ������Һ�����뼸����ˮ���ټ����������Ȼ�̼�����ã����Ȼ�̼�����ɫ��
����ȡ������Һ����μ���NaOH��Һ��ʹ��Һ�������ʼ��ԣ�Ȼ���ټ���Na2CO3��Һ���а�ɫ�������ɡ�
��������ʵ�������ƶ�ԭ��Һ�У�
��1���϶����ڵ������� ��
��2���϶������ڵ������� ��
��3�����ܴ��ڵ������� ��
��4��д��������з�����Ӧ�����ӷ���ʽ ��
�ο��𰸣���8�֣���1��H+��Ba2+��I������2��SO42����CO3
���������
�������������pH��ֽ���飬����Һ��ǿ���ԣ�˵����H+����CO32������ȡ������Һ�����뼸����ˮ���ټ����������Ȼ�̼�����ã����Ȼ�̼�����ɫ��˵����I��������ȡ������Һ����μ���NaOH��Һ��ʹ��Һ�������ʼ��ԣ�Ȼ���ټ���Na2CO3��Һ���а�ɫ�������ɣ�˵����Ba2+����SO42����
���㣺�������ӵļ��鷽�� ���ӹ�������
�������ж���Һ�������ܷ�Ĺ���Ϊ��
1��һɫ--��Һ��ɫ
������ɫ��Һ����ͭ���ӡ����������ӡ����������ӡ�����������ӵ�����ɫ�����Ӳ����ڣ�
2������--��Һ�����ԡ�����
����ǿ������Һ�У����������Ӽ���������Ӳ��ܴ������ڣ�
����ǿ������Һ�У������Ӻ����������Ӳ��ܴ������ڣ�
���������ʽ���������ǿ���Ի�ǿ������Һ�о����ܴ������ڣ�
3��������--�������
��ƫ�����������̼��������Ӳ��ܹ��棻
����������Ӻ���������Ͼ���ǿ�����ԣ�
4���ķ�Ӧ--���ַ�Ӧ����
�����Ӧ�����Ӳ��ܹ��森
�ٸ��ֽⷴӦ
��������ԭ��Ӧ
����ٽ���ˮ�ⷴӦ
����Ϸ�Ӧ
�����Ѷȣ�����
3��ѡ���� �����£�������Һ��һ���ܴ����������������
A�����д���Fe3+����Һ��SO32-��Na����Cl����SO42��
B����ʹ��������Ѹ���ܽ����Һ��Na+��Fe2+��NO3����SO42��
C��ˮ���������c(H��)��1��10��12mol��L����Һ��SO42-��NH4����Cl����Ca2+
D��pH=0����Һ��NH4����Na����SO42����Fe3+
�ο��𰸣�D
������������Ӽ������ʽ������ԭ��Ӧ�����ܴ������棬��֮�ǿ��Եġ�A����ȷ����Ϊ������������SO32����B����Һ���������ԣ�Ҳ�����Լ��ԡ���������ԣ���NO3��������Fe2��������Լ��ԣ���Fe2�����ܴ������棻ͬ��C����Һ���������ԣ�Ҳ�����Լ��ԣ�����Ca2����SO42�����ܴ������棬���Դ�ѡD��
�����Ѷȣ�һ��
4��ѡ���� ����������������Һ���ܴ����������
A��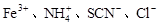
B��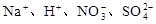
C��Al3����Fe2+��NO3-��Cl��
D��K����Na����Cl����SiO32��
�ο��𰸣�B
���������
���������
A��Fe3+��SCN-�����γ��������Բ��ܴ������棬��A�������⣻
B��������֮�䲻�������ӷ�Ӧ����������Һ�о��ܴ������棬��B�������⣻
C��Fe2+��NO3-��������Һ�����д���H+���ڵ���Һ�п��Է���������ԭ��Ӧ�����ܹ��棬��C�������⣻
D��SiO32����H+���Է�Ӧ���ɹ�����������ܴ������棬��D�������⡣
���㣺�������ӷ�Ӧ�����ӹ���
���������⿼�������ӷ�Ӧ�����ӹ������⣬�Ѷ��еȡ�����ʱӦע�����Ӳ�����ļ������ͣ���1���ֽⷴӦ�������棬��������С�ࣺ���������ﲻ�ܹ��棻�������岻�ܹ��棻�����ѵ������ˮ�����ᣬ�����2����������ԭ��Ӧ�������棬��Ҫ���������ӵ��������뻹ԭ�����ǿ����������Fe3+��I-���ܹ��棻��3�����γ������������档��Fe3+��SCN-��
�����Ѷȣ�һ��
5��ѡ���� ��ˮ��Һ���ܴ��������һ����
A��NH4+��Ag+��CO32����SO42��
B��Fe2+��H+��MnO4����HCO3��
C��K+��Na+��NO3����SO42��
D��Al3+��Mg2+��C1����SiO32��
�ο��𰸣�C
���������
�����������������̼������ӡ���������ӷֱ�Ӧ������̼������������������������A�����������ӡ������������������������������������ԭ��Ӧ�����������ӡ������Ӻ�ˮ������������̼����������ܷ���˫ˮ�ⷴӦ�����������������Ͷ�����̼���壬��������̼�������������Ӧ�����ɶ�����̼�����ˮ����B����K+��Na+��NO3����SO42��֮�䲻�ܷ�����ѧ��Ӧ����C��ȷ�����������������Ӷ���ˮ�⣬��ٽ��Է���ˮ�⣬�����ܷ���˫ˮ�ⷴӦ���������������������������þ��������������Ҳ�ܷ���˫ˮ�ⷴӦ��
�����Ѷȣ���