微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。 已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能( kJ/mol) P-P:198,P-O: 360,O=O:498。则反应P4(白磷)+3O2 = P4O6的能量变化为
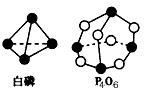 [???? ]
[???? ]
A.释放1638 kJ的能量
B.吸收l 638 kJ的能量
C.释放126 kJ的能量
D.吸收126 kJ的能量
2、选择题 以NA代表阿伏加德罗常数,则关于反应:C2H2(g)+2/5O2(g)=2CO2 (g )+H2O(l) △H=-1300kJ/mol热化学方程式的说法正确的是[???? ]
A.有10NA个电子转移时,该反应放出1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量
C.有2NA个碳氧共用电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
3、填空题 在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热。已知0.4mol液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64kJ的热量。
(1)在结构上N2H4和NH3的关系有如H2O2和H2O的关系。N2H4能发生下列反应:
N2H4+H3O+=N2H5++H2O
N2H4+H2O N2H5++OH-
N2H5++OH-
N2H5++H2O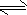 N2H62++OH-
N2H62++OH-
N2H5++H2O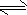 N2H4+H3O+
N2H4+H3O+
据此可得出的结论是______________。
A.肼水解显酸性
B.肼在水中可电离出H+离子
C.肼是二元弱碱
D.肼是二元弱酸
(2)写出肼和H2O2反应的热化学方程式_______________________。
(3)已知H2O(1)==H2O(g) △H=+44kJ/mol,则16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是___________________________。
(4)上述反应应用于火箭推进器,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是
_____________________。
(5)用氨和次氯酸钠按一定的物质的量之比混合可生成肼,写出反应的化学方程式__________________________,该反应的还原产物是___________________。
4、选择题 已知某管道煤气的主要成分是H2和CO,天然气的主要成分是CH4,它们燃烧的热化学方程式为
2H2(g)+O2(g)=2H2O(l) △H=-571. 6kJ/mol
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890. 31kJ/mol
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的可燃气体,理论上所获得的热量,后者大约是前者的多少倍
[???? ]
A.0.8
B.1.3
C.1.6
D.3.1
5、选择题 已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol
CO(g)+1/2O2(g)=CO2(g)△H=-282.5kJ/mol
假如标准状况下由CH4、CO、CO2组成的89.6L混和气体完全燃烧时能放出1010kJ的热量,并生成18g液态水,那么燃烧前混和气体中CO所占的体积百分含量为( ? )