微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有关钠的叙述不正确的是(???)
A.少量钠应保存在煤油中,实验后剩余的钠需放回原瓶
B.2.3g钠与97.7g 水反应后溶液中溶质的质量分数大于4%
C.钠与CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出的金属铜
D.用一般的化学还原法不能制取金属钠,但可用电解熔化NaCl的方法制得
参考答案:C
本题解析:
试题分析:A、少量钠应保存在煤油,可防止钠与空气中的O2、水分反应,为了安全,剩余的钠需放回原瓶,正确;B、2.3g钠与97.7g 水反应后,生成4g NaOH,因为生成了氢气,溶液的质量小于100g,所以溶质的质量分数大于4%,正确;C、Na与H2O反应生成NaOH,NaOH再与Cu2+反应生成Cu(OH)2,因Na与H2O发生的反应是放热反应,反应放出的热导致生成的Cu(OH)2表面部分分解为CuO(黑色)而非Cu,错误;D、金属钠不能用还原法制取,但用电解熔融的NaCl的方法可制取金属钠,正
本题难度:简单
2、选择题 如图是工业制纯碱的部分物质转化示意图,下列推测错误的是
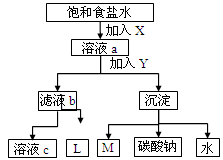
A.若是联碱法,溶液c可在转化流程中循环利用
B.若是氨碱法,则L的主要成分是NaCl
C.M可在转化流程中循环利用
D.X是NH3,Y是CO2
参考答案:AB
本题解析:
试题分析:A、若是联碱法,则X是氨气,Y是CO2,c是氯化铵溶液不能在转化流程中循环利用,A不正确;B、若是氨碱法,则L的主要成分是CaCl2,B不正确;C、M是CO2可以循环利用,C正确;D、由于氨气极易溶于水而CO2在水中的溶解性不大,所以X是NH3,Y是CO2,D正确,答案选AB。
本题难度:一般
3、填空题 (12分)某研究性学习小组在网上搜集到信息:钾、钙、钠、镁等活泼金属能在CO2气体中燃烧。他们对钠在CO2气体中燃烧进行了下列实验:
?操作过程
| 实验现象
|
将干燥的玻璃燃烧匙中燃烧的钠迅速
伸入到盛有装满CO2的集气瓶中
| 钠在盛有CO2的集气瓶中继续燃烧
|
反应后冷却
| 集气瓶底附着黑色颗粒,瓶壁上附着有白色
物质
???(1)要熄灭燃烧的钠,可以选用的物质是____??????(填字母)
a.水??? b.泡沫灭火剂??? c.干沙土??? d.二氧化碳
(2)该小组同学对瓶壁上的白色物质的成分进行讨论并提出假设
I.白色物质是Na2O;
II.白色物质是Na2CO3;
III.白色物质还可能是????????????
(3)
实验步骤
| 实验现象
| ①取少量白色物质于试管中,加入适量水,振荡,样品全
部溶于水,向其中加入过量的CaCl2溶液
| 出现白色沉淀
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液
| 无明显现象
??? ①通过对上述实验的分析,你认为上述三个假设中,____????????成立。
②写出该反应的方程式?????????????????????????????????来源:91考试网 91exam.org?????????。
参考答案:
 本题解析: 本题解析:
试题分析:⑴由于钠能与水、氧气、CO2等反应,故选用干沙土熄灭燃烧的钠;
⑵根据已知的假设I和Ⅱ,可提出假设Ⅲ为“白色物质还可能是Na2O和Na2CO3的混合物”;
⑶①据实验步骤①可确定生成物中含有Na2CO3,据实验步骤②可确定生成物中没有Na2O,故假设Ⅱ成立;
②该反应的反应物有Na、CO2,生成物有Na2CO3、C,最后根据氧化还原反应的配平方法将其配平。
本题难度:一般
4、填空题 (10 分)(1)明矾的组成为??????????????????,明矾的用途??????????,其在水中的电离方程式是??????????????????????????????????????????。
(2)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为 ? 。
参考答案:(每空2分)(1) KAl(SO4) 2 ・ 12H2O,净
本题解析:
试题分析:(1)明矾的化学式是KAl(SO4) 2 ・ 12H2O。明矾溶于水能生成氢氧化铝胶体,因此可以用作净水剂。电离方程式是KAl(SO4) 2=K++Al3++2SO42-。
(2)碳酸氢钠不稳定,受热易分解,生成碳酸钠、水和CO2,所以除去Na2CO3粉末中混入的NaHCO3杂质用加热的方法,反应的化学方程式是2NaHCO3 本题难度:一般 本题难度:一般
5、选择题 下列物质均有漂白作用,其漂白原理相同的是 [???? ]
①过氧化钠
②次氯酸
③二氧化硫
④活性炭
⑤ 臭氧
A.①②③
B.①③⑤
C.①②⑤
D.②③④
参考答案:C
本题解析:
本题难度:简单
|
|