微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将Na2O2投入到FeCl2溶液中,可观察到的现象是
①有气泡产生?②生成白色沉淀?③生成红褐色沉淀?④无变化
A.①、③
B.①、②
C.①、②、③
D.④
参考答案:A
本题解析:
试题分析:过氧化钠溶于水生成氢氧化钠和氧气,溶液显碱性,且过氧化钠还具有强氧化性。所以将Na2O2投入到FeCl2溶液中,可观察到的现象是有气泡产生。亚铁离子被氧化生成铁离子,然后与生成的氢氧化钠反应生成红褐色氢氧化铁沉淀,因此正确的答案选A。
本题难度:一般
2、选择题 9.2g金属钠投入到足量的H2O中,则产生的气体中含有
A.0.2mol中子
B.0.4mol电子
C.0.2mol质子
D.0.4mol分子
参考答案:B
本题解析:略
本题难度:一般
3、填空题 (8分)食盐和工业用盐具有广泛的用途。已知,工业盐含NaNO2,外观酷似食盐并有咸味。NaNO2有氧化性和还原性,遇酸分解放出NO2。
(1)下列试剂可鉴别工业盐和食盐的是?????????
a. H2O??? b.酸性高锰酸钾溶液??? c.盐酸
(2)NaNO2与氢碘酸反应(含氮产物为NO)的离子方程式为???????.
(3)某工厂废液中含有2%―5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就 能使NaNO2中的氮转化为对空气无污染的气体,该物质是??????????
能使NaNO2中的氮转化为对空气无污染的气体,该物质是??????????
a.NaCl?????????????????? b.NH4Cl??????????????? c.浓H2SO4
(4)氯碱工业通过电解饱和食盐水来获得相应的产物。请写出电解食盐水的离子方程式?????????????。
参考答案:
 本题解析:略
本题解析:略
本题难度:一般
4、选择题 将0.01 mol下列物质分别加入100 mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①Na2O2 ②Na2O ③Na2CO3 ④NaCl
A.①>②>③>④
B.①>②>④>③
C.①=②>③>④
D.①=②>③=④
参考答案:C
本题解析:0.01 mol Na2O2、Na2O与水反应的方程式分别为Na2O2+H2O=2NaOH+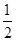 O2↑、Na2O+H2O=2NaOH,二者均产生0.02 mol OH-,因溶液体积变化忽略不计,故所得溶液中阴离子浓度:①=②;Na2CO3和NaCl电离产生的阴离子均为0.01 mol,而CO32―发生微弱的水解:C
O2↑、Na2O+H2O=2NaOH,二者均产生0.02 mol OH-,因溶液体积变化忽略不计,故所得溶液中阴离子浓度:①=②;Na2CO3和NaCl电离产生的阴离子均为0.01 mol,而CO32―发生微弱的水解:C
本题难度:一般
5、选择题 在一定温度下,向饱和烧碱溶液中加入一定量的过氧化钠,充分反应后恢复到原温度,下列说法错误的是
A.溶液中Na+数目减少,有固体析出
B.溶液中Na+数目减少,有气体逸出,
C.溶液中H2O数目减少,溶质的质量分数增大
D.溶液中H2O数目减少,溶质的质量分数未变
参考答案:C
本题解析:
试题分析:过氧化钠与水反应生成氢氧化钠和氧气,饱和烧碱溶液中水减少,溶质的质量分数不变,会析出NaOH固体,Na+数目减少,故C项错误。
本题难度:一般