微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 定条件下,存在可逆反应X(g)+2Y(g)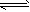 3Z(g),若X、Y、Z起始浓度分别为
3Z(g),若X、Y、Z起始浓度分别为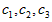 (均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是[???? ]
(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是[???? ]
A.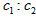 =l:2
=l:2
B.达平衡状态时,生成Z的速率是生成X速率的3倍
C.X、Y的转化率不相等
D.C2的取值范围为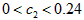
参考答案:C
本题解析:
本题难度:一般
2、选择题 反应2SO2+O2 ??2SO3在一定温度下达到平衡,下列说法正确的是(?? )
??2SO3在一定温度下达到平衡,下列说法正确的是(?? )
A.增大压强,平衡向右移动,平衡常数K增大
B.此时一定满足c(SO2)=2c(O2)
C.增加O2的浓度平衡向右移动,SO2的转化率增大
D.平衡向右移动时反应物的浓度减小,生成物的浓度增大
参考答案:C
本题解析:平衡常数只与温度有关系,改变压强,平衡常数不变,A不正确;平衡时SO2和氧气的浓度不再发生变化,但二者不一定满足2倍的关系,B不正确;增大氧气的浓度,平衡向正反应方向移动,SO2的转化率增大,C正确;D不正确,平衡向正反应方向移动,反应物的浓度不一定减小,生成物的浓度不一定增大,答案选C。
本题难度:一般
3、选择题 反应A+3B=2C+D在四种不同情况下的反应速率分别为:
①v(A) =0.15mol/(L・s) ②v(B)=0.6mol/(L・s) ③v(C)=0.5mol/(L・s) ④v (D) =0.45mol/(L・s)
则反应进行由快到慢的顺序为[???? ]
A.④>③>①>②
B.②>④>③>①
C.②>③>④>①
D.④>③>②>①
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列情况下,反应速率相同的是 [???? ]
A.等体积0.1 mol/L HCl和0.1 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应
B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应
参考答案:C
本题解析:
本题难度:一般
5、选择题 将反应Cu (s) + 2Ag+ (aq)  ?Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是
?Cu2+ (aq) + 2Ag (s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,有关叙述正确的是
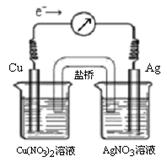
A.KNO3盐桥中的K+移向Cu(NO3)2溶液
B.当电流计指针为0时,该反应达平衡,平衡常数K=0
C.若此时向AgNO3溶液中加入NaCl固体,随着NaCl量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
D.若此时向Cu(NO3)2溶液中加入NaOH固体,随着NaOH量的增加电流计指针向右偏转幅度减小→指针指向0→向左偏转
参考答案:C
本题解析:
试题分析:A、根据电子流向,Cu为负极,而KNO3盐桥中的K+移向正极,错误;B、该反应达平衡时各物质的量不在变化,也不会有能量的变化,所以电流计指针为0,但平衡常数不为0,错误;C、随着NaCl量的增加,Ag+的浓度下降,反应速率减小(电流计指针向右偏转幅度减小)直到建立平衡(指针指向0),Ag+的浓度再下降,会使平衡逆移(向左偏转),正确;D、NaOH量的增加,正反应速率不变,电流计指针向右偏转幅度不变,错误。
本题难度:一般