微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 银锌电池广泛用作各种电子仪器的电源,其电极分别是Ag2O和锌,电解液为KOH溶液。电池反应是:Ag2O+Zn+H2O="2Ag" +Zn(OH)2,根据上述判断:
(1)原电池的正极是__________,负极是__________。
(2)原电池电极反应式为:负极_______________,正极______________。
(3)工作时原电池负极附近溶液的pH__________ (填“增大”、“不变”、“减小”)。
参考答案:(5分)(1)Ag2O,??? Zn。
(2)Zn+
本题解析:
试题分析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据方程式可知,锌失去电子,作负极。氧化银得到电子,做正极。
(2)负极锌失去电子,电极反应式是Zn+ 2OH--2e-=Zn(OH)2。正极氧化银得到电子,电极反应式是Ag2O+H2O+2e-=2Ag+ 2OH-。
(3)根据负极电极反应式可知,工作时原电池负极消耗OH-,所以附近溶液的pH减小。
点评:该题是基础性试题的考查,侧重
本题难度:一般
2、选择题 人造地球卫星用到一种高能电池--银锌蓄电池,其电极反应式为: Zn+2OH--2e-==ZnO+H2O,
Ag2O+H2O+2e-==2Ag+2OH-。据此判断氧化银(Ag2O)是 [???? ]
A.负极,被氧化
B.正极,被氧化
C.负极,被还原
D.正极,被还原
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列有关铜锌原电池(下图)的叙述正确的是
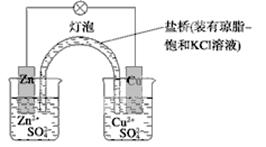
A.正极反应为Zn-2e-===Zn2+
B.取下盐桥,原电池仍可工作
C.在外电路中,电子从正极流向负极
D.电池反应为Zn+Cu2+===Zn2++Cu
参考答案:D
本题解析:
试题分析:A、锌比铜活泼,锌是负极失去电子,A错误;B、取下盐桥,不能形成闭合回路,原电池不能再工作,B错误;C、在外电路中,电子从负极流向正极,C错误;D、正极是铜,溶液中的铜离子放电,总反应式为Zn+Cu2+=Zn2++Cu,D错误,答案选D。
考点:考查原电池原理的应用与判断
本题难度:一般
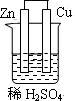
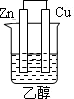
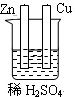
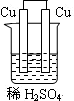
4、选择题 下列为原电池装置的是
 ??
?? ????
???? ???
???
A??????????? B????????? C????????? D
参考答案:A
本题解析:考查原电池的构成,构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入到电解质溶液中,所以A正确。B中乙醇是非电解质,C中没有用导线相连,D中电极是同一种金属,且和稀硫酸不反应,答案选A。
本题难度:一般
5、选择题 观察下列几个装置示意图,有关叙述错误的是(????)
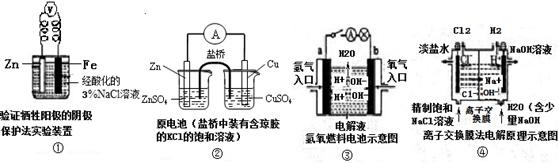
A.装置①中烧杯内中加入黄色的K3[Fe(CN)6]溶液,一段时间后看不到Fe电极附近有蓝色沉淀生成,该装置可看作金属的析氢腐蚀
B.装置②盐桥中的Cl―向硫酸铜溶液移动
C.装置③中外电路电流方向:b极 →a极
D.装置④中阳极反应:2 Cl――2e- = Cl2 ↑
参考答案:B
本题解析:
试题分析:A、装置①是原电池装置,锌作负极,铁作正极,亚铁离子遇到K3[Fe(CN)6]溶液有蓝色沉淀生成,看不到现象说明铁没有被氧化,电解质溶液显酸性,因此发生析氢腐蚀,正确;B、装置②是双液电池,锌作负极,铜作正极,盐桥中阴离子移向负极,向左移,错误;C、装置③是燃料电池,氢气作负极,氧气作正极,电流从正极流向负极,正确;D、装置④是电解池,阳极阴离子失电子发生氧化反应,正确。
本题难度:一般