Al与CuCl2溶液反应,生成了H2和Cu(OH)2
参考答案:AD
本题解析:略
本题难度:一般
2、实验题 (8分)某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.00 mL于锥形瓶中,加入10.00 mL KI溶液(足量),滴入指示剂2―3滴。
②取一滴定管依次用自来水、蒸馏水洗净,然后注入0.01 mol・L-1Na2S2O3溶液(显碱性),调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2 + 2Na2S2O3?=" 2NaI" + Na2S4O6。
试完成下列问题:
(1)步骤①加入的指示剂是____________________。
(2)步骤②应使用____________式滴定管。
(3)步骤③当待测液由___________色变为__________色且不再变化即达终点,若耗去Na2S2O3溶液40.00 mL,则废水中Cl2的物质的量浓度为__________________________。
(4)以上实验步骤中有一处明显的操作错误,请指出.??????????????????????????
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
3、简答题 用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中.当滴到最后一滴时红色突然褪去.试回答下列问题:
(1)实验室保存饱和氯水的方法是______.
(2)请写出新制饱和氯水中含有氯元素的物质的化学式______.
(3)产生上述现象的原因可能有两种(简要文字说明):①是由于______;②是由于______.
简述怎样用实验证明红色褪去的原因是①或者②?
______.
参考答案:(1)氯水是液体,应用细口瓶盛装;氯水中HClO光照易分解,
本题解析:
本题难度:一般
4、计算题 BaCl2・xH2O中结晶水数目可通过重量法来确定:
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和????????????洗涤沉淀;检验沉淀中氯离子是否洗净的方法是????????????。
(2)计算BaCl2・xH2O中的x=??????????(要求写出计算过程)。
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果??????????(填“偏低”、“偏高”或“不变”)。
参考答案:
(1)蒸馏水取水洗液于试管中,加入稀硝酸酸化,滴加A
本题解析:
(1)洗涤沉淀,需要用蒸馏水冲洗;若沉淀洗涤后洗涤液中不含Cl―则已经洗净,然后检验滤液中是否含有Cl―即可。
(2)计算氯化钡和水的物质的量比,即求出x;
样品中BaCl2的物质的量为n(BaCl2)= 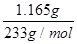 =5.000×10-3mol =5.000×10-3mol
质量m(BaCl2)=5.000×10-3mol×208g/mol=1.040g
n(H2O):n(BaCl2)= 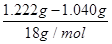 :(5.000×10-3mol)=2.02≈2 :(5.000×10-3mol)=2.02≈2
(3)题中已经表明硫酸钡被还原为BaS,则沉淀质量减小,相对水的质量比提高,x数据将偏高。
【考点定位】本题考查BaCl2・xH2O中结晶水数目的测定。
本题难度:一般
5、实验题 如下图是甲同学设计的证明CO具有还原性的实验装置。

回答下列问题:
(1)实验时应先点燃___(填“A”或“B”)处的酒精灯。
(2)洗气瓶中的现象为________。
(3)酒精灯B的作用是____。
(4)乙同学提出甲设计太复杂,可将酒精灯合二为一,去掉B 而将尾气导管口旋转到A的火焰上即可,乙同学设计是否合理?____;理由是________。
(5)丙同学质疑CO能否使澄清石灰水变浑浊,因此其设计在CO通入CuO之前应先通过澄清石灰水以排除CO与澄清石灰水反应,试对此做出评价,你认为丙的设计____ (填“必要”或“不必要”)理由是________。
(6)丁同学认为甲设计的装置中尾气处理还可以用其他方法,请你为丁同学设计一种合理的尾气处理方法:___。
参考答案:(1)B
(2)澄清石灰水变浑浊
(3)将未反
本题解析:
本题难度:一般
|