微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题
卤代烃是一类重要的有机合成中间体,是许多有机合成的原料。根据卤代烃的相关性质,回答下列问题
(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为?????????????????????????????,请预测B的核磁共振氢谱上应该有?????????????个峰(信号)。

(2)某同学用如图1装置(铁架台、酒精灯等略)验证取代反应和消去反应的产物。
 ????
????
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和0.5 mL溴乙烷振荡。
实验操作Ⅱ:将试管如图1固定后,水浴加热。
①据图1:用水浴加热而不直接用酒精灯加热的原因是???????????。
②图2是为证明溴乙烷在NaOH乙醇溶液中发生的是消去
反应,实验中需要检验的产物是????????????????????????,
水的作用是??????????????????????????????????????????,
实验现象是??????????????????????????????????????????。
参考答案: 本题解析:
本题解析:
试题分析:(1)据图可知只有一个峰,故说明A物质只有一种等效氢.A的同分异构体有两个不等效氢,所以会有两个峰(2)水浴加热主要的作用使反应物均匀受热(3)溴乙烷在NaOH乙醇溶液发生消去反应的产物主要是乙烯,所以需要检验的产物就是乙烯。而在反应中乙醇沸点较低,容易挥发,所以乙醇也会随着产物蒸发出来,且乙醇液能使高锰酸钾溶液褪色,乙醇易溶于水中所以水的主要作用就是出去乙烯中的乙醇,防止干扰乙烯的检验。乙烯可以使高锰酸钾溶液褪色,所以可选用高锰酸钾溶液。
本题难度:一般
2、选择题 下列说法不正确的是???????????????????????????????(??)
A.对硝基甲苯的结构简式为 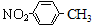
B.“地沟油”禁止食用,但可以用来制肥皂
C.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
D.H2(g) +Cl2(g)==2HCl(g)△H=-184.6 kJ/mol不是氢气的燃烧热方程式
参考答案:A
本题解析:
试题分析:A、对硝基甲苯的结构简式为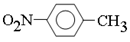 ,A不正确;B、“地沟油”中含有对人体有害的物质禁止食用,由于地沟油的主要成分是油脂,可以用来制肥皂,B正确;C、升高温度,一般可使活化分子的百分数增大,因而反应速率增大,C正确;D、燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,因此H2
,A不正确;B、“地沟油”中含有对人体有害的物质禁止食用,由于地沟油的主要成分是油脂,可以用来制肥皂,B正确;C、升高温度,一般可使活化分子的百分数增大,因而反应速率增大,C正确;D、燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,因此H2
本题难度:一般
3、简答题 某含氧有机化合物可以作为无铅汽油的抗暴剂。它的蒸气密度是同温同压下CO2的2倍,含碳的质量分数为68.2%,含氢的质量分数为13.6%,红外光谱和核磁共振显示该分子有4个甲基,通过计算推导出分子式和结构简式。
参考答案:C5H12O(1分)?? (CH3)3C―O―CH3(2分)
本题解析:
试题分析:该有机物的蒸气密度是同温同压下CO2的2倍
则该有机物的相对分子质量M=2×44=88
1 mol化合物中含有n(C)=(88×68.2%)÷12=5mol
n(H)=(88×13.6%)÷1=12 mol
所以n(O)=(88×18.2%)÷16=1 mol
因此分子式为C5H12O
由于红外光谱和核磁共振显示该分子有4个甲基
所以该有机物的结构简式为(CH3)3C―O―CH3
本题难度:一般
4、实验题 3,5?二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5?二甲氧基苯酚的部分物理性质见下表:
物质
| 沸点/℃
| 熔点/℃
| 密度(20 ℃) /g・cm-3
| 溶解性
|
甲醇
| 64.7
| ―
| 0.791 5
| 易溶于水
|
乙醚
| 34.5
| ―
| 0.713 8
| 微溶于水
|
3,5?二甲氧基苯酚
| ―
| 33~36
| ―
| 易溶于甲醇、乙醚,微溶于水
?
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是________________。②萃取用到的分液漏斗使用前需________并洗净,分液时有机层在分液漏斗的________(填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是________;用饱和食盐水洗涤的目的是________________________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是________(填字母)。
a.蒸馏除去乙醚? b.重结晶
c.过滤除去干燥剂? d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先________,再________。
参考答案:(1)①蒸馏 ②检查是否漏水 上
(2)除去HCl 除
本题解析:(1)甲醇和3,5?二甲氧基苯酚是互溶的,可以利用两者的沸点不同,用蒸馏的方法进行分离。使用分液漏斗时首先要对分液漏斗进行是否漏水的检查。由于乙醚的密度比水小,所以有机层在分液漏斗的上层。
(2)由于在合成时所用的是氯化氢的甲醇溶液,所以加NaHCO3溶液的目的是除去HCl,用饱和食盐水洗涤的目的是除去少量的NaHCO3杂质,同时可以减少3,5?二甲氧基苯酚的损失。
(3)洗涤后,产物中仍混有H2O和乙醚,所以先加入无水CaCl2除去H2O,然后过滤除去CaCl2。通过蒸馏除去乙醚,最后重结晶
本题难度:一般
5、选择题 某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,并且a<b,则x、y、z必须满足的关系是
A.x>z
B.x="y=z"
C.x="z"
D.x<z
参考答案:A
本题解析:略
本题难度:一般
|