微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式正确的是
A.铜片插入硝酸银溶液中 Cu+Ag+==Cu2++Ag
B.硫酸钠和氯化钡溶液反应 Ba2++SO42-=BaSO4↓
C.澄清石灰水与稀盐酸反应 Ca(OH)2+2H+==Ca2++2H2O
D.碳酸钙与盐酸反应 CO32― + 2H+ = CO2↑ + H2O
参考答案:B
本题解析:
试题分析:A、电荷不守恒,应为Cu+2Ag+==Cu2++2Ag,错误;B、Ba2++SO42-=BaSO4↓,正确;C、澄清石灰水是溶液Ca(OH)2应拆开,应为OH-+H+="=" H2O,错误;D、碳酸钙不拆开,应为Ca CO3+ 2H+ = Ca2++CO2↑+ H2O
考点:离子方程式的书写。
本题难度:一般
2、选择题 下列离子方程式书写正确的是
A.往CaCl2溶液中通入少量的CO2: Ca2++CO2+H2O==CaCO3↓+2H+
B.向碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+ OH-==CO32-+ H2O
C.向AlCl3溶液中加入过量的浓氨水:Al3++4NH3・H2O=A1O2-+4NH4++2H2O
D.向Ba(OH)2溶液中加入少量的NaHSO3溶液:HSO3-+Ba2++OH-==BaSO3↓+H2O
参考答案:D
本题解析:
试题分析:A项CaCO3能溶于盐酸,所以反应不能发生;B项因为氢氧化钠溶液过量,所以NH4+和HCO3-都发生反应:HCO3-+ 2OH-+NH4+==CO32-+2 H2O+NH3.↑ C项Al(OH)3只溶于强碱溶液,所以离子方程式应为:Al3++3NH3・H2O=A1(OH)3↓+3NH4+;
考点:离子方程式的书写。
本题难度:困难
3、填空题 (12分)用一种试剂除去下列物质中的杂质(括号中为杂质),写出所用试剂及离子方程式。
(1)Na2SO4溶液(CuSO4)
除杂试剂: ,离子方程式: 。
(2)FeCl2溶液(CuCl2)
除杂试剂: ,离子方程式: 。
(3)Fe(Al)
除杂试剂: ,离子方程式: 。
参考答案:(12分,每空2分)(1)NaOH溶液,Cu2++2OH-=
本题解析:
试题分析:(1)硫酸铜能和氢氧化钠溶液反应生成蓝色程度氢氧化铜,据此可以除去硫酸钠中的硫酸铜,反应的离子方程式是Cu2++2OH-= Cu(OH)2↓。
(2)铁能和氯化铜反应生成氯化亚铁和铜,所以除去氯化亚铁中的氯化铜,可以加入铁,反应的离子方程式是Fe+ Cu2+=Fe2++ Cu。
(3)铝能溶于氢氧化钠溶液中,而铁不能,所以加入的试剂是氢氧化钠溶液,反应的离子方程式是2Al+2OH-+2H2O = 2AlO2-+3H2↑。
考点:考查物质的分离和提纯
点评:把物质中混有的杂质除去而获得纯净物叫提纯,将相互混在一起的不同物质彼此分开而得到相应组分的各纯净物叫分离。在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。
本题难度:一般
4、填空题 (16分)氮及其化合物在化学实验中有广泛应用:
(1)请写出实验室用Cu和稀硝酸反应制备NO的离子方程式: ;
(2)请设计实验,检验某可溶性固体物质中含有NH4+的操作、现象、结论: ;
(3)实验室可用(NH4)2Cr2O7受热分解产生N2、Cr2O3和H2O来制备N2,请写出该分解反应的化学方程式: ;
(4)有人发现重铬酸铵分解产物不仅含N2、Cr2O3和H2O,还含有NH3和O2,并指出伴随有显著的副反应发生:2(NH4)2Cr2O7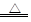 2Cr2O3+4NH3↑+2H2O+3O2↑;设计如下图所示实验装置,并通过实验方法验证了NH3和O2的存在(忽略空气中O2的干扰)。
2Cr2O3+4NH3↑+2H2O+3O2↑;设计如下图所示实验装置,并通过实验方法验证了NH3和O2的存在(忽略空气中O2的干扰)。

限选试剂:Na2S溶液、Na2SO3溶液、FeSO4溶液;
限选仪器:试管、玻璃导管、漏斗、烧杯、胶头滴管
①图中试管口玻璃纤维的作用是 ;
②根据实验目的,选择一种试剂和最佳的仪器补全该实验装置(在方框中画图并标注所选试剂);
③写出该法验证NH3和O2存在的实验原理的化学方程式: 。
参考答案:(1)3Cu+8H++2NO3-===3Cu2++2NO↑+
本题解析:
试题分析:(1)Cu和稀硝酸反应制备NO的离子方程式为:3Cu+8H++2NO3-===3Cu2++2NO↑+4H2O。(2)NH4+的检验通常是加强碱将其转化为NH3,再检验NH3,具体操作为:取少量待测固体(或先配制成浓溶液亦可)于试管中,加入过量浓的NaOH溶液,加热,在试管口放置湿润的红色石蕊试纸,产生无色有刺激性气味的气体,且试纸变蓝,则原溶液含有NH4+。(3)(NH4)2Cr2O7受热分解产生N2、Cr2O3和H2O,知道了反应物和生成物,则化学方程式为:(NH4)2Cr2O7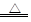 Cr2O3+N2↑+4H2O。(4)①加热时固体物质可能下来堵塞导管,在气体检验时气体的流速均匀有利于实验的操作,故试管口玻璃纤维的作用是:缓冲气流,防止固体被气流带进入导管,堵塞导管。②要检验NH3和O2根据所提供的试剂最好选FeSO4溶液,实验现象明显,NH3溶于水使的溶液显碱性,碱性溶液中FeSO4会生成Fe(OH)2,Fe(OH)2溶液被O2氧化生成红褐色的Fe(OH)3,有气体反应为了防止溶液倒吸,需要采取防倒吸的装置,则装置为:
Cr2O3+N2↑+4H2O。(4)①加热时固体物质可能下来堵塞导管,在气体检验时气体的流速均匀有利于实验的操作,故试管口玻璃纤维的作用是:缓冲气流,防止固体被气流带进入导管,堵塞导管。②要检验NH3和O2根据所提供的试剂最好选FeSO4溶液,实验现象明显,NH3溶于水使的溶液显碱性,碱性溶液中FeSO4会生成Fe(OH)2,Fe(OH)2溶液被O2氧化生成红褐色的Fe(OH)3,有气体反应为了防止溶液倒吸,需要采取防倒吸的装置,则装置为:
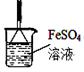
③根据上述分析NH3和O2与FeSO4反应的化学方程式为:2NH3+2H2O+FeSO4=Fe(OH)2↓+(NH4)2SO4;4Fe(OH)2+O2+2H2O=4Fe(OH)3
考点:化学方程式的书写、物质的检验试剂的选择、实验装置的绘制。
本题难度:困难
5、填空题 用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出反应的离子方程式。
(1)FeSO4(CuSO4):
所需试剂(填化学式) ,所涉及的离子方程式: 。
(2)O2(CO2):
所需试剂(填化学式) ,所涉及的离子方程式: 。
参考答案:(1)FeSO4(CuSO4):
所需试剂(填化学式)
本题解析:略
本题难度:一般