微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
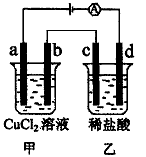
1、选择题 按下图所示装置进行电解,电极材料均为石墨。下列说法正确的是
 [???? ]
[???? ]
A. b的电极反应为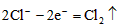
B. d的电极反应为
C. a、c两极产生气体的物质的量相等
D. 甲、乙两烧杯中溶液的pH均保持不变
参考答案:C
本题解析:
本题难度:一般
2、选择题 在标准状况下,用铂电极电解CuSO4溶液,当阴极产生12.8g铜时,阳极放出的气体是(???)
A.1.12LH2
B.1.12LO2
C.2.24LH2
D.2.24LO2
参考答案:D
本题解析:
试题分析:用铂电极电解CuSO4溶液的化学方程式为2CuSO4+ 2H2O  2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
本题难度:一般
3、填空题 铁及其化合物在日常生活、生产中应用广泛.研究铁及其化合物的应用意义重大.
I.水体的净化和污水的处理与铁及其化合物密切相关.
(1)自来水厂常用高铁酸钠(Na2FeO4)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理 .
(2)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
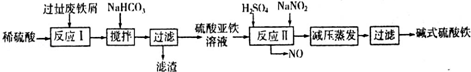
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
|
开始沉淀
| 2.3
| 7.5
| 3.4
|
完全沉淀
| 3.2
| 9.7
| 4.4
回答下列问题:
①写出反应I中主要发生的氧化还原反应的离子方程式 .
②加入少量NaHCO3的目的是调节溶液pH,应控制pH的范围为 .
③在实际生产中,反应II常同时通入O2以减少NaNO2的用量,若通入5.6L O2(标准状况),则相当于节约NaNO2的质量为 g.
④碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成[Fe2(OH)4]2+聚合离子.该水解反应的离子方程式为 .
II铁的化合物也是制备高能锂电池的重要原料.已知磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式 . LiFePO4,电池中的固体电解质可传导Li+.试写出该电池充电时的阳极反应式 .
参考答案:Ⅰ.(1)FeO42
本题解析:
本题难度:困难
4、选择题 如图a、b、c、d均为石墨电极,通电进行电解。下列说法不正确的是???????
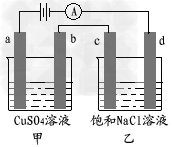 [???? ] [???? ]
A.甲中a电极反应式为4OH--4e-=O2↑+2H2O
B.当b极有64gCu析出时,c电极产生2g气体
C.电解后向乙中通入适量HCl气体,溶液组成可以恢复
D.电解时向乙中滴入酚酞试剂,d电极附近变红
参考答案:B
本题解析:
本题难度:一般
5、填空题 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应为???????????????????????。
在X极附近观察到的实验现象是?????????????????????。
②Y电极上的电极反应式为??????????????????????。
检验该电极反应产物的方法是????????????????????????????????????????。
参考答案:.①2H++2e- = H2↑电极表面产生大量气泡,溶液颜色
本题解析:
试题分析:①电解池中X极和电源的负极相连,做阴极,溶液中的氢离子放电生成氢气,电极反应式为2H++2e- = H2↑。由于氢离子放电,破坏了阴极周围水的电离平衡,所以溶液显碱性,则实验中观察到的现象是电极表面产生大量气泡,溶液颜色变红。
②Y电极和电源的正极相连,做阳极,溶液中的氯离子放电,则电极反应式为2Cl- + 2e- = Cl2↑。氯气具有强氧化性,据此可以鉴别,即检验该电极反应产物的方法是使湿润的淀粉碘化钾试纸变蓝。
点评:该题是基础性试题的考查,试题紧扣教材基础上,旨在巩固
本题难度:一般
|