微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关化学反应速率的说法中,正确的是
A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B.用铁片和稀硫酸反应制取氢气,改用铁片和浓硫酸可以加快产生氢气的速率
C.在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体可加快溶液褪色速率
D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,为了加快反应速率,实际生活中使用了增大压强或升高温度的方法。
参考答案:C
本题解析:
试题分析:A、100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,溶液体积增大,氢离子浓度减小,生成氢气的速率变慢,错误;B、浓硫酸和铁发生钝化,不会产生氢气,错误;C、在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体做该反应的催化剂,可加快溶液褪色速率,正确;D、汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,为了加快反应速率,实际生活中使用了加催化剂的方法,错误。
本题难度:一般
2、选择题 下列过程中,需要减慢化学反应速率的是( )
A.炼钢
B.炼铁
C.合成纤维
D.食物腐败
参考答案:炼钢、炼铁以及合成纤维等工业生产,为提高产量,都需要提高反应
本题解析:
本题难度:简单
3、选择题 下列有关说法正确的是
A.锌与稀硫酸反应时加入少量硫酸铜,反应加快的原因是Cu2+水解增大了H+浓度
B.增大醋酸溶液的浓度,溶液中c(OH-)减小的原因是水的离子积Kw减小
C.pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱
D.TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加
参考答案:D
本题解析:
试题分析:A、锌与硫酸反应时加少量硫酸铜,锌置换出铜,形成原电池,加快反应速率,错误;B、水的离子积随温度变化而变化,错误;C、pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明氢氧化锂是弱碱,错误;TATP受撞击自发反应,△H≈0,说明反应△S>0,正确。
本题难度:一般
4、选择题 A与B在容积为1 L的密闭容器中发生反应:aA(s)+bB(g) cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:

下列说法正确的是
A.0~t1时间段内,平均反应速率v(B)=O.04/t1 mol・(L・min)-1
B.若起始时n(D)=0,则t2时v(D)=0.20/t2 mol・(L・min)-1
C.升高温度,v(B)、vC)、v(D)均增大
D.b:d=6:1
参考答案:C
本题解析:
试题分析:A. B的起始量不可知,无法求出0~t1min内的平均速率。B. v(D)=0.20/t2 mol・(L・min)-1为0~t1时间段内平均速率而非t1时刻的瞬时速率。故B错。C.升高温度,化学反应速率增大,正确。D.由表中数据可得:t1到t2时间段内
aA(s)+bB(g)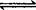 cC(g)+dD(g)
cC(g)+dD(g)
△n /mol 0.06 0.06 0.1
所以:b:c:d=3:3:5 故D错误。
考点:了解化学反应速率的概念、反应速率的定量表示方法;理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识其一般规律。
本题难度:一般
5、实验题 (8分)某化学反应2A (g)  ?B(g) + D(g) 在4种不同条件下进行,B和D的起始浓度为0 ,反应物A 的浓度(mol?L-1) 随反应时间 (min) 的变化情况如下表:
?B(g) + D(g) 在4种不同条件下进行,B和D的起始浓度为0 ,反应物A 的浓度(mol?L-1) 随反应时间 (min) 的变化情况如下表:
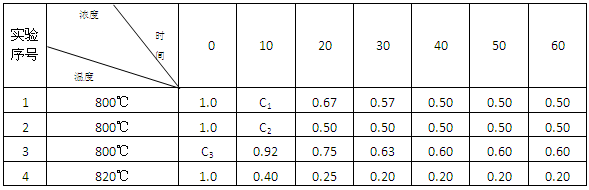
根据上述数据,完成下列填空:
(1)实验1达到平衡的时间是???????min,实验4达到平衡的时间是???????min.
(2)C1??????????????C2(填“大于”“小于” “等于”);C3= ????????????mol?L-1
(3)实验4比实验1的反应速率?????(填“快”或“慢”),原因是????????????????
(4)如果2A (g)  ?B(g) + D(g) 是一个放热反应,那么实验4与实验1相比,?????放出的热量多,理由是??????????。
?B(g) + D(g) 是一个放热反应,那么实验4与实验1相比,?????放出的热量多,理由是??????????。
参考答案:(1)40???? 30??(2)大??大于1.0
(
本题解析:(1)当反应达到平衡状态后,各种物质的浓度和含量将不再发生变化。根据表中数据可知实验1和实验4在分别反应进行到40min和30min时A的浓度就不再随时间变化而变化,这说明反应已经达到化学平衡状态。
(2)实验1和实验2相比温度相同,起始浓度相同,到达平衡时A的浓度也相同,但到达平衡的时间是实验2用时少,这说明实验2的反应速率大,进行的快,因此1.0-C1<1.0-C2,所以C1>C2。因为随着反应的进行,A的浓度逐渐减小,所以反应速率会逐渐减小,即C3-0.92mol/L>0.92mol/L-0.
本题难度:一般