��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij����ѧ��ѧ��ȤС��������ͼ��ʾԭ���װ�ý���ʵ�飬��ش��������⣺

��1��ʵ���У�ͬѧ�Ƿ�����װ�õ����Ƶ�ָ��ƫת����ͬ���������������¹۵㣬������ȷ����____________����˫ѡ�⣬©ѡ��2�֣���ѡ��ѡ��0�֣�
A�������������þǿ
B���������þ����ǿ����װ����þ��Ϊ����
C�������ݽ������˳����ȷ�ж�ԭ��ص�������
D��ԭ����е��������ܵ������Һ������ԡ�ǿ�����Ե����ص�Ӱ��
��2��Ҫȷ�ж�ԭ��ص����������˿��õ����Ƶ��DZ������⣬������ͨ���۲��������жϣ���д����ͼ�еĵ缫���ϼ���Ӧ������þ����Ϊ����������
������?????????????????������?????????????????????????????????????��
��3��д����ͼ�еĵ缫��Ӧʽ��
�ٸ�����?????????????_________________________��
�������� ?????????????_________??????__________??��
��4����ͼ����Ƭ��NaOH��Һ��Ӧ�����ӷ���ʽΪ___________________________________��ijͬѧ�����ͼ��ʵ��ǰ��Ƭ��������5g��ʵ����������2.3g������ʵ������в������������Ϊ_______���������ת�Ƶ��ӵ����ʵ���Ϊ________��
�ο��𰸣���17�֣���1��С��3�֣�����ÿ��2�֣�
��1��C��D
���������
�����������1����װ���У��������ϡ���ᣬ�������ǿ�Ľ����Ǹ�������װ���е����������������Һ������þ������������Һ����Ӧ������Ϊ������������þ�����������Դ�ѡCD��
��2���������Ǹ�����ʧȥ���ӣ����ܽ⡣þ����������������������ɡ�
��3����ͼ��þ�Ǹ�����������������缫��Ӧʽ�ֱ��Ǹ������ĵ缫��Ӧʽ��Mg��2e�D��Mg2�� ��������2H+��2e�D��H2����
��4����ͼ����Ƭ��NaOH��Һ��Ӧ�����ӷ���ʽΪ2Al+2OH��+2H2O��2AlO2-+3H2������ͼ��ʵ��ǰ��Ƭ
�����Ѷȣ�һ��
2��ѡ���� ��ť�۵�����ִ��������й㷺Ӧ�ã���һ����п��أ���缫�ֱ���Ag2O��Zn���������ҺΪKOH���缫��ӦΪ��Zn+2OH--2e=ZnO+H2O��Ag2O+H2O+2e=2Ag+2OH-������������Ӧʽ���ж�������������ȷ���ǣ�������
A����ʹ�ù����У���ظ�������Һ��pH��С
B��ʹ�ù����У�������Ag20�������·����Zn��
C��Zn�Ǹ�����Ag2O������
D��Zn�缫������ԭ��Ӧ��Ag2O�缫����������Ӧ
�ο��𰸣�A����������Zn+2OH--2e=ZnO+H2O��c��OH-
���������
�����Ѷȣ���
3��ѡ���� ���з�Ӧ�У���ԭ���Ͽ�����Ƴ�ԭ��ص���
A��Ba(OH)2��8H2O��NH4Cl�ķ�Ӧ
B����Ƭ��Ũ����ķ�Ӧ
C�������������ķ�Ӧ
D��ʯ��ʯ�ķֽⷴӦ
�ο��𰸣�C
���������ԭ������е�������������ֻ��������ԭ��Ӧ������Ƴ�ԭ��أ�B�����ۻ���AD����������ԭ��Ӧ�������ȷ�Ĵ�ѡC��
�����Ѷȣ���
4��ѡ���� ������ͼ��ʾ��ԭ��أ�����˵����ȷ����
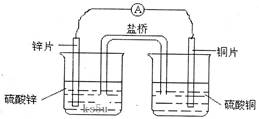
A�����Ӵ�п�缫ͨ������������ͭ�缫
B�������е�������������ͭ��Һ��Ǩ��
C��п�缫������ԭ��Ӧ��ͭ�缫����������Ӧ
D��ͭ�缫�Ϸ����ĵ缫��Ӧ��2H++e-��H2��
�ο��𰸣�
A
���������
���⿼��ԭ��ص�ԭ����п��������ͭƬ�����������ӴӸ�������������Aѡ����ȷ�����������ƶ���Bѡ�����������������Ӧ������������ԭ��Ӧ��Cѡ�����ͭ�缫�����ķ�ӦΪCu2����2e��=Cu��Dѡ�����
�����Ѷȣ�һ��
5��ѡ���� �ճ����øɵ�صĵ缫�ֱ�Ϊ̼����пƤ���Ժ�״NH4Cl��ZnCl2������ʣ����м���MnO2��������H2�����缫��Ӧ�ɼ�Ϊ��Zn-2e-=Zn2+��2NH4++2e-=2NH3+H2��NH3�����ڽ��Zn2+�����������������ж�����˵������ȷ���ǣ�������
A���ɵ����ZnΪ������̼Ϊ����
B���ɵ�ع���ʱ��������Zn�������·����̼��
C���ɵ�س�ʱ������ʹ��ʱ��װ��״�����������ʴ����
D���ɵ�ؿ���ʵ�ֻ�ѧ������ܵ�ת���͵�����ѧ�ܵ�ת��
�ο��𰸣�A���ɵ���нϻ��õĽ���п���������ϲ����õĵ���ķǽ���̼��
���������
�����Ѷȣ���