��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��д��ȷ����(???? )
A���������к�����������Һ�ķ�Ӧ��OH-��H+�� H2O
B��������ͨ���Ȼ�������Һ��2Fe2++Cl2��2Fe3++2Cl��
C����������������������Һ��Al+2OH����AlO2��+H2��
D������ϡ���ᷴӦ��2Fe+6H+��2Fe3++3H2��
2��ѡ���� ���л�ѧ����ʽ�����ӷ���ʽ����ȷ���ǣ�???��
A��S��Cu��Ӧ Cu+S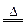 CuS
CuS
B��������ù�����pH��С 2H2SO3+O2�T2H2SO4
C�������������Һ������ʯ��ˮ���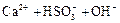 �TCaSO3��+H2O
�TCaSO3��+H2O
D����Na2S��Na2SO3�Ļ����Һ�еμ�ϡH2SO4[n(Na2S)��n(Na2SO3)=2��1]
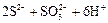 �T3S����3H2O
�T3S����3H2O
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��д��ȷ����[???? ]
A���Ȼ�ͭ��Һ�����۷�Ӧ��Cu2++Fe=Fe2++Cu
B��ϡH2SO4�����۷�Ӧ��2Fe+6H+=2Fe3++3H2��
C������������Һ��ϡH2SO4��Ӧ��Ba2++SO42-==BaSO4��
D��̼��������ᷴӦ��CO32-+2H+==H2O+CO2��
4������� �ҹ���ҽҩ������ǧ����ʷ������ص���Чʹ�þ���ӹ�����ҩ��Ʒ����������г����������ڽ�����ҩʱ����ҩ���ؽ���Ԫ�غ��ж�Ԫ�صĺ����ȸ���ָ�����Ƿdz��ϸ�ģ���˰Ѻó�����ҩ���������Ƿdz���Ҫ�ġ����½����˷���ʵ���Ҷ��в�ҩ�п��ܵIJ����ж�Ԫ��As�ļ��鷽���Ͳ��裨As���в�ҩ����Ҫ��As2O3����ʽ���ڣ���
��ȡ1000g�в�ҩ��Ʒ����ǰ�ڴ����Ƶô�����Һ����ʱ��Ʒ�п��ܺ��е�AsԪ�ؽ�ת��ΪH3AsO3��
�ڽ�������Һת����250mL��ƿ�У�������2��3��0.2%�ĵ�����Һ��
���ñ�����Һ�ζ�������Һ���յ㣬����20.25mL��I2��Һ����䷢����Ӧ��
H3AsO3�� I2�� H2O��H3AsO4��? I���� H����δ��ƽ��
�Իش��������⣺
��1��������ζ��������в�ҩ��Ʒ����ǰ�ڴ����Ƶô�����Һ��
???????????????????????????????????????????????????????????????????????��
��2����ƽ���ӷ�Ӧ����ʽ��__H3AsO3��__I2��__H2O�� __H3AsO4��__I����__H��
��3��0.2%�ĵ�����Һ��������??????������жϵζ������յ㣿?????????????��
��4���������ñ�����Һ���ǽ��ⵥ��ֱ���ܽ�������ˮ���Ƶã�������0.1070g��KIO3��������KI�Լ����ϣ�������ȷϡ�͵�1000 mL���Ƶã�����һ�����ӷ�Ӧ����ʽ˵��������Һ���γɹ���?????????????????????????????????????��
��5���ҹ���ҩ��ֲ�P�Ƽ���������ɫ��ҵ������������ɫ��ҩ���麬��������2.000mg/kg���Լ���˵�����в�ҩ��Ʒ�Ƿ�ϸ����������̣������֪����Ʒ�麬��ԼΪ???????mg/kg���ʸò�ҩ��Ʒ???????����ϸ��ϸ���
5��ѡ���� ���б�ʾˮ������ӷ���ʽ��ȷ���ǣ�
A��CH3COO�� + H2O CH3COOH + OH��
CH3COOH + OH��
B��NH4+ + H2O NH4OH + H+
NH4OH + H+
C��S2- + 2H2O H2S+2OH-
H2S+2OH-
D��HCO3- + H2O  H3O++CO32-
H3O++CO32-