微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 用98%的浓硫酸(密度为1.84g/cm3)配制1mol/L的稀硫酸100mL,回答下列问题:
(1)量取浓硫酸的体积为______mL.
(2)配制时需选用的仪器主要有量筒、烧杯、玻璃棒、______.
(3)转移后用少量蒸馏水洗涤烧杯2~3次,否则,所制溶液物质的量浓度会______(偏大、偏小、无影响).
(4)定容时若俯视刻度线,所得溶液的浓度______(偏大、偏小、无影响).
参考答案:(1)浓H2SO4的物质的量浓度c=
本题解析:
本题难度:一般
2、选择题 瓦斯中甲烷与氧气的质量比为1:4时,极易爆炸,此时甲烷与氧气的体积比为
A.1:4
B. 1:2
C.1:1
D.2:1
参考答案:B
本题解析:
试题分析:甲烷与氧气的质量比为1:4,根据n=m/M,则物质的量之比是1/16:4/32="1:2," 此时甲烷与氧气的体积比也是物质的量之比为1:2,答案选B。
考点:考查物质的质量比与物质的量之比的计算
本题难度:一般
3、填空题 下图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为???????mol・L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是????????。
A.溶液中HCl的物质的量??????? B.溶液的浓度
C.溶液中Cl-的数目???????????? D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400 mol/L的稀盐酸。
①该学生需要量取??????mL上述浓盐酸进行配制。
②配制溶液除烧杯和玻璃棒,还需要的仪器是??????、??????、???????。
③实验开始时,需要检查????????????????????。
④配制时,下列操作正确的顺序是(用字母表示)???????????????????????。
A.洗涤??????B.定容??????C.溶解????D.摇匀????E.冷却????F.称量???? G.转移
⑤在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填“偏大”、“偏小”或“无影响”)。
Ⅰ.用量筒量取浓盐酸时俯视观察凹液面(???? )
Ⅱ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水(???? )
Ⅲ.配制时,容量瓶有少量蒸馏水(???? )]
Ⅳ.定容时仰视刻度线(???? )
参考答案:(1) 11.9mol/L????? (2) BD?????
本题解析:
试题分析:(1) 直接根据公式计算: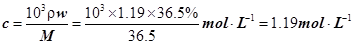 。(2) A、溶液中HCl的物质的量=nV,所以与溶液的体积有关,A不合题意;B、溶液的浓度
。(2) A、溶液中HCl的物质的量=nV,所以与溶液的体积有关,A不合题意;B、溶液的浓度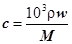 本题难度:一般
本题难度:一般
4、选择题 配制一定物质的量浓度的稀盐酸时,最后用胶头滴管向容量瓶滴加蒸馏水,由于不慎,液面超过了容量瓶颈上的刻度,这时应采取的措施是(???)
A.用胶头滴管吸出超过的那一部分
B.把溶液倒出一部分在蒸发皿中,蒸发一部分水后把蒸发皿中剩余的溶液仍注入容量瓶,重新加水至刻度
C.根据超出的蒸馏水量,经过计算,补加浓盐酸
D.把容量瓶中的溶液全部弃去,重新配制。
参考答案:D
本题解析:
试题分析:液面超过了容量瓶颈上的刻度,这时应采取的措施是把容量瓶中的溶液全部弃去,重新配制,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查。该题的关键是明确物质的量浓度溶液配制的原理、操作注意事项,然后灵活运用即可,有利于培养学生的规范严谨的实验设计能力和动手操作能力。
本题难度:一般
5、填空题 200 mL 0.2 mol・L-1和100 mL 0.5 mol・L-1的两种盐酸混合,设得到300 mL盐酸,其物质的量浓度是________。若所得盐酸的密度为1.004 g・cm-3,则其溶质的质量分数是____。
参考答案:0.3 mol・L-1??1.09%
本题解析:c(HCl)=
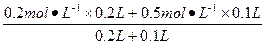 =
=
0.3 mol・L-1
w(HCl)= 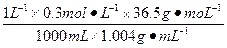 ×100%=1.09%
×100%=1.09%
本题难度:简单