微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列变化,不包含化学变化的是(??)
A.煤焦油的分馏
B.煤的干馏
C.煤的气化
D.煤的液化
参考答案:A
本题解析:略
本题难度:简单
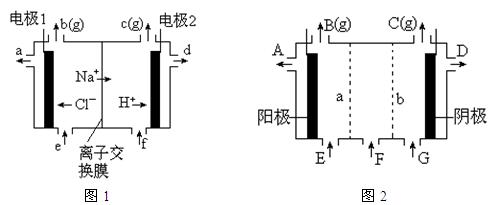
2、填空题 图1是氯碱工业中离子交换膜电解槽示意图,其中离子交换膜是“阳离子交换膜”,它有一特殊的性质――只允许阳离子通过而阻止阴离子和气体通过。
⑴、工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为?▲?,?▲?。
⑵、如果粗盐中SO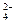 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO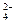 ,该钡试剂可以是?▲?。
,该钡试剂可以是?▲?。
A.Ba(OH)2???????B.Ba(NO3)2??????C.BaCl2?
⑶、为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为?▲?。
A.先加NaOH,后加Na2CO3,再加钡试剂?
B.先加NaOH,后加钡试剂,再加Na2CO3???
C.先加钡试剂,后加NaOH,再加Na2CO3
⑷、电解后得到的氢氧化钠溶液从?▲?口流出,b口排出的是?▲?气体,电极1应连接电源的
?▲?极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是?▲?。
⑸、图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。请回答:
①、a为?▲?(填“阳”、“阴”)离子交换膜。
②、阳极的电极反应式是?▲?。
③、从D、E口流出或流进的物质的化学式分别为?▲?,?▲?。
参考答案:⑴、Ca2++CO 本题解析:略
本题解析:略
本题难度:一般
3、选择题 根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
①CaBr2+H2O CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2↑
HgBr2+H2↑
③HgBr2+CaO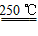 HgO+CaBr2 ④2HgO
HgO+CaBr2 ④2HgO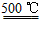 2Hg+O2↑
2Hg+O2↑
该方案的目的是为了制备[???? ]
A.HBr
B.CaO
C.H2
D.Hg
参考答案:C
本题解析:
本题难度:简单
4、填空题 用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。
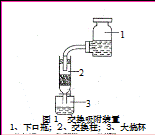
①浸泡海带:取海带500g,加13~15倍水量分两次浸泡,得浸出液6000mL左右,碘含量为0.5g/L。?
②碱化浸出液除褐藻糖胶:即海带浸出液1000mL,加入浓度为40% 的NaOH溶液,控制pH值为12左右,充分搅拌后使褐藻酸钠絮状沉淀而沉降。采用倾析法分离出清液。
③氧化游离:向上述清液中加入浓度为6mol× L-1的H2SO4溶液,使pH值为1.5~2。往酸化后溶液中加入NaClO溶液或H2O2溶液,充分搅拌并观察溶液颜色变化。待溶液由淡黄逐渐变成棕红色即表明I-离子已转变为多碘离子(I3-)。
④交换吸附:氯型强碱性阴离子交换树脂(R―Cl表示)注入交换柱中(树脂层高度为12cm),如右图连接交换装置,待溶液全部通过后,树脂颜色变为黑红色。
⑤洗脱:分两步进行
第一步:取8~10% 的NaOH溶液40mL注入交换柱中。在强碱作用下,树脂颜色逐渐变浅,待树脂基本褪色后,放出溶液,收集于一小烧杯中为碱性洗脱液。????
第二步:取10% 的NaCl溶液40mL注入上述交换柱中。稍待一会儿,慢慢放出溶液收集于另一小烧瓶中,为氯化钠洗脱液。
⑥往碱性洗脱液中滴加H2SO4溶液(6mol/L),烧杯底部会析出一层泥状粗碘。
⑦往氯化钠洗脱液中滴加H2SO4溶液(6mol/L)使之酸化,再滴加10% 的NaNO2溶液(在通风橱中进行)。待溶液由无色转变为棕红色直至出现棕黑色浑浊。
⑧离心分离即得粗碘。
试回答下列问题
(1)步骤③在酸性条件下用NaClO(或H2O2)氧化碘的离子方程式:?? ? ?,
及I2 +I-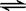 I3-。如何用化学方法检验有多碘离子生成?????????????????????。
I3-。如何用化学方法检验有多碘离子生成?????????????????????。
(2)第④步发生的离子反应为:????????????????????????????。
(3)步骤⑤洗脱时第一步发生的离子反应为(洗脱液中含有I-和IO3-离子):
???????????;第二步洗脱发生的离子反应为:?????????????????。
(4)步骤⑦发生反应的离子方程式为 ????????????????????????????????。
参考答案:
(1)2I-+ClO-+2H+ = I2+Cl-+H
本题解析:
本题考查用离子交换法从海带中提取碘。(1)NaClO(或H2O2)在酸性条件下有强氧化性,将I-氧化成I2;(2)离子交换的原理,根据颜色变化可知,I3-交换Cl-,方程式为R-Cl+I3-= R-I3+Cl- ;(3)在强碱作用下,树脂颜色逐渐变浅,根据洗脱液中含有I-和IO3-离子,说明R-I3转化为I-和IO3-,方程式为:3R-I3+6OH- = 3R-I+5I-+IO3-+3H2O;加入Cl-与I-交换,R-I+Cl- = R-Cl+I-;(4)在酸性条件下NO2-具有氧化性,将I-氧化
本题难度:一般
5、填空题 硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3?MgO、CaO等,生产工艺流程示意如下:
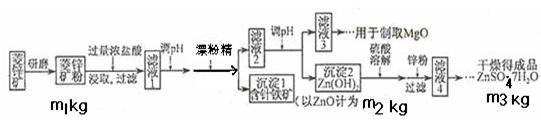
(1)将菱锌矿研磨成粉的目的是____??_,滤液1后两步操作的目是:??????????????????。
(2)完成加漂粉精反应的离子方程式:
□Fe(OH)2+□____+□_____ →□Fe(OH)3+□Cl-
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据
????????????????????????,????????????????????????(用文字叙述)
(5) “滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
参考答案:(共12分,每小题2分)1)增大反应物接触面积或增大反应速率
本题解析:略
本题难度:一般