微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 CH3COOH溶液中存在如下平衡:CH3COOH?H++CH3COO-,加入少量下列固体物质能使平衡向左移动的是( )
A.NaCl
B.CH3COONa
C.Na2CO3
D.NaOH
参考答案:A、氯化钠和醋酸不反应也没有相同的离子,所以不能使平衡向左移
本题解析:
本题难度:一般
2、选择题 下列物质中属于电解质的是
A.CuSO4
B.Al
C.石墨
D.蔗糖
参考答案:A
本题解析:分析:电解质是指:该物质是化合物,溶于水溶液中或在熔融状态下就能够导电,是自身电离,在水溶液中和在熔融状态下两种情况下都不能导电的化合物称为非电解质,据此即可解答.
解答:A.硫酸铜水溶液中或在熔融状态下有自由移动的铜离子和硫酸根离子,能导电,硫酸铜是化合物,是电解质,故A正确;
B.Al是金属是单质,能导电,它既不是电解质也不是非电解质,故B错误;
C.石墨虽能导电,但它是单质,它既不是电解质也不是非电解质,故C错误;
D.蔗糖是化合物,在水溶液中和熔融状态下只存在蔗糖分子,没有自由移动的离子,所以不能导电,是非电解质,故D错误;
故选A.
点评:本题是对基本概念电解质的考查,题目难度不大,平时学习注意概念的辨析、基础知识的积累.
本题难度:一般
3、选择题 25℃时,用浓度为0.1000mol?L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol?L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)=
Ka(HY)?c(HY)
c(Y-)
+c(Z-)+c(OH-)
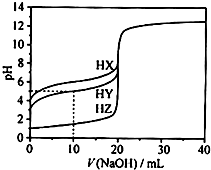
参考答案:A、氢氧化钠体积为0时,0.1000mol?L-1的三种酸H
本题解析:
本题难度:简单
4、选择题 常温下将体积都为10mL、pH都等于3的醋酸和盐酸,加水稀释至a mL和b mL,测得稀释后溶液的pH均为5,则稀释后溶液的体积为 ( )
A.a>b
B.a<b
C.a="b=100mL"
D.a=b=100mL
参考答案:A
本题解析:略
本题难度:一般
5、填空题 硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:
H2SO4=H++HSO4-,HSO4- H++SO42-。 H++SO42-。
请回答下列有关问题:
(1)K2SO4溶液呈 ____________ (填“弱酸性”、“中性”或“弱碱性”),其理由是_____________________________(用离子方程式表示)。
(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为________________________________。
(3)若25℃时,0.10 mol・L-1的NaHSO4溶液中c(SO42-)="0.029" mol・L-1,则HSO4-的电离常数Ka="____________" (保留两位有效数字);0.10 mol・L-1的H2SO4溶液中c(H+)____________ 0.129mol・L-1(填“>”、“=”或“<”)。
参考答案:
本题解析:
试题分析:(1)由于SO42-+H2O HSO4-+OH-,故K2SO4溶液呈弱碱性;(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为HSO4-+HCO3-=H2O+CO2↑+SO42-;(3)NaHSO4溶液中存在硫酸氢根离子的电离平衡:HSO4-?H++SO42-,其Ka=[H+]?[SO4 HSO4-+OH-,故K2SO4溶液呈弱碱性;(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为HSO4-+HCO3-=H2O+CO2↑+SO42-;(3)NaHSO4溶液中存在硫酸氢根离子的电离平衡:HSO4-?H++SO42-,其Ka=[H+]?[SO4
本题难度:一般
|