微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4==Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
[???? ]
????????? 反应温度/℃??????????? Na2S2O3溶液?????????????????? 稀H2SO4??????????????? H2O
????????????????????????????????? ? V/mL?????c/(mol・L-1)??????? V/mL????c/(mol・L-1)??????? V/mL?
A?????????? 25??????????????????? ?5???????????? 0.1???????????????? 10????????????0.1????????????????? 5
B???????????25???????????????????? 5?????????????0.2????????????????? 5?????????????0.2???????????????? 10
C?????????? 35??????????????????? ?5??????????? ?0.1?????????????????10??????????? 0.1????????????????? 5
D?????????? 35???????????????????? 5?????????????0.2????????????????? 5???????????? 0.2???????????????? 10
参考答案:D
本题解析:
本题难度:一般
2、填空题 将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol・L-1・s-1,则在2 s时,容器中有???mol A,此时C的物质的量浓度为????????。
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol・L-1・s-1,则在2 s时,容器中有???mol A,此时C的物质的量浓度为????????。
参考答案:8.8 0.08 mol・L-1
本题解析:3A(g)? +B(g)? 2C(g)
2C(g)
起始浓度(mol・L-1):? 1.0??? 0.5??? 0
转化浓度(mol・L-1):? 0.06×2=0.12? 0.04?? 0.08
2 s时浓度(mol・L-1):? 1.0-0.12="0.88" 0.5-0.04="0.46" 0.08<
本题难度:简单
3、实验题 (7分)污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物。某小组同学拟探究H2C2O4浓度对反应速率的影响。
实验仪器
I.实验原理
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
II.实验设计
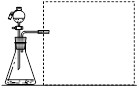
(1)【方案一】测量气体产物:在相同温度下,利用下图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响)。下图方框中应选择 (填编号)仪器组装量气装置,限选以下仪器:
①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒、⑦秒表。
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间。拟定实验数据:
实验序号
| 温度/℃
| 各物质的体积 / mL
| 反应时间
|
H2O
| 3 mol/L稀硫酸
| 0.1mol/L KMnO4溶液
| 0.6 mol/LH2C2O4溶液
|
1
| 25
| 3.0
| 2.0
| 4.0
| 6.0
| t1
|
2
| 25
| ①
| 2.0
| 4.0
| 4.0
| t2
|
3
| ②
| 7.0
| 2.0
| 4.0
| 2.0
| t3
表中①、②处的数据分别是 、 。
III.讨论与交流
(3)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如下图所示。他们认为:0~t时间内,速率变快的可能原因是 。
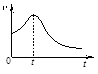
(4)实验室常用KMnO4标准溶液滴定某浓度草酸。KMnO4溶液置于 (填仪器名称)中,判断到达滴定终点的现象是 。若滴开始时,滴定管中有气泡,滴定结束时气泡消失,则测定结果 (填“偏高”、“偏低”、“无影响”)。
参考答案:(1)③⑤⑥或①②④⑤⑥
(见右图)
本题解析:
试题分析:(1)用排水法测量气体的体积,如图所示: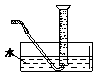 ,所需仪器有③水槽、⑤导管、⑥量筒或如图所示: ,所需仪器有③水槽、⑤导管、⑥量筒或如图所示: ,所需仪器有①广口瓶、②双孔塞、④橡胶管、⑤导管、⑥量筒;(2)在相同温度下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间,实验时溶液的体积相同,H2C2O4的浓度不同,则②应为25℃,由①③数据可知溶液总体积为15mL,则①为5mL;(3)影响化学反应速率的因素主要有温度、浓度、压强和催化剂,反应为放热反应,温度升高,且生成的锰离子对反应可能起到催化作用,都可加快反应速率,随着反应的进行,浓度逐渐降低,此时反应速率又减小,答案为:①产物Mn2+是反应的催化剂、②该反应放热使温度升高;(4)高锰酸钾具有腐蚀性,应放在酸式滴定管中,达到滴定终点时,溶液由无色变为浅紫红色,且半分钟内不褪色;若读取滴定管数据时,起始读数正确,终点仰视读数,导致所读体积偏大,即需要的高锰酸钾的体积偏大,则测定的浓度偏高。 ,所需仪器有①广口瓶、②双孔塞、④橡胶管、⑤导管、⑥量筒;(2)在相同温度下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间,实验时溶液的体积相同,H2C2O4的浓度不同,则②应为25℃,由①③数据可知溶液总体积为15mL,则①为5mL;(3)影响化学反应速率的因素主要有温度、浓度、压强和催化剂,反应为放热反应,温度升高,且生成的锰离子对反应可能起到催化作用,都可加快反应速率,随着反应的进行,浓度逐渐降低,此时反应速率又减小,答案为:①产物Mn2+是反应的催化剂、②该反应放热使温度升高;(4)高锰酸钾具有腐蚀性,应放在酸式滴定管中,达到滴定终点时,溶液由无色变为浅紫红色,且半分钟内不褪色;若读取滴定管数据时,起始读数正确,终点仰视读数,导致所读体积偏大,即需要的高锰酸钾的体积偏大,则测定的浓度偏高。
考点:考查探究影响化学反应速率的因素。
本题难度:困难
4、选择题 用铁片与稀硫酸反应制取氢气时,下列措施可以使氢气生成速率加大的是
? [???? ]
A.加入少量的硫酸钠
B.加入硝酸钠固体
C.滴加少量CuSO4溶液
D.改用浓硫酸
参考答案:C
本题解析:
本题难度:一般
5、实验题 (9分)某学生用0.1×10×25mm3,质量分数≥99.5%的铝片和盐酸反应制取H2,实验现象见下表:

(1)写出铝片与盐酸、硫酸反应的离子方程式??????????????????????????????????
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,15~20min内,反应速率逐渐减小。其原因是????????????????????????????????????????????????????????????
(3)①根据铝片与盐酸和硫酸反应现象的差异,有学生对此现象提出如下猜想(至少要写出两种假设):
假设一:Cl-对该反应有促进作用,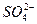 对该反应不影响。 对该反应不影响。
假设二:????????????????????????????????????????????????????????????。
假设三:????????????????????????????????????????????????????????????。]
假设四:????????????????????????????????????????????????????????????。
③?请你以“假设一”为实验课题,设计实验方案探究,要求写 出主要实验步骤。 出主要实验步骤。
????????????????????????????????????????????????????????????????????
??????????????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????
????????????????????????????????????????????????????????????????????
参考答案:
 本题解析:本题属于开放性试题,要求学生结合具体的实验情境,作出推断和假设,设问角度新颖,考查学生了解科学研究的基本思路和方法。(3)中答案也可能多种多样。如“ 本题解析:本题属于开放性试题,要求学生结合具体的实验情境,作出推断和假设,设问角度新颖,考查学生了解科学研究的基本思路和方法。(3)中答案也可能多种多样。如“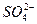 对金属铝与H+反应有抑制作用”或“ 对金属铝与H+反应有抑制作用”或“ 本题难度:一般 本题难度:一般
|