��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��100 mL 0.1 mol��L-1���������[��NH4��2Fe��SO4��2]��Һ����ε���0.1 mol��L-1 Ba��OH��2��Һ������Ba��OH��2��Һ���V�ı仯,���������ʵ���n�ı仯��ͼ��ʾ��������˵������ȷ���ǣ��� ����
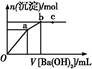
A��a��ʱ��Һ��������Ҫ����Ϊ��NH4��2SO4
B��a��b�η�����Ӧ�����ӷ���ʽ��:S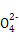 +Ba2+
+Ba2+ BaSO4��
BaSO4��
C��b��Ϊ��������,��Ӧ��������ֵΪ0.02
D��c�����Ba��OH��2��Һ�����Ϊ200 Ml
�ο��𰸣�A
���������O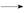 a�η����ķ�ӦΪ:Fe2++S
a�η����ķ�ӦΪ:Fe2++S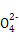 +Ba2++2OH-
+Ba2++2OH- �����Ѷȣ�һ��
�����Ѷȣ�һ��
2������� ��ÿ��2�֣���10�֣�ij��Һ�н������±��е�һЩ���ӣ�������ˮ�ĵ�������ӵ�ˮ�⣩
������
| Na+?? Mg2+?? Fe2+??? Al3+??Fe3+??????
|
������
| OH-???Cl-???CO32-??NO3-?? SO42-????
Ϊ������Щ���ӣ�ȡ������Һ����ϡHCl������ɫ�������ɡ���������������Ϊ����ɫ������Һ�������ӵ�����䣻
��1��ͨ��������ʵ�飬��ȷ����Һ��һ�����ڵ�������������������һ�����ڵ�������������������������
��2��д��ʵ���з��������ӷ���ʽ???????????????????????��
��3��ͨ����ʵ��ķ������в���ȷ����Һ���Ƿ���ڵ���������?????????����ν�һ������������Ƿ����???????????��
�ο��𰸣���ÿ��2�֣���10�֣�(1��(1��? Fe2+???????
�������������ϡHCl������ɫ�������ɡ���������������Ϊ����ɫ������������NO����˵�����������NO3��������������ԭ��Ӧ�����һ�������������ӣ���Ͳ��ܺ���OH����CO32����������Һ�������ӵ�����䣬����һ�����������ӣ���SO42������ȷ����Ҫȷ��SO42����������������ữ���Ȼ������м��飬��ȡ����ԭ��Һ,���������ữBaCl2��Һ,��������ɫ��������֤����SO42-��
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��д��ȷ����
A��̼�������ϡ���CO32�D + 2H+ �� CO2��+ H2O
B���Ȼ�ͭ��Һ�м���NaHS��Һ�� Cu2+ + HS�D �� CuS��+ H+
C��̼������Һ��ͨ������������̼��CO32�� + CO2 + H2O �� 2HCO3��
D�����������Һ�м�����������������Һ��NH4+ + OH�D �� NH3��+ H2O
�ο��𰸣�BC
�����������
�����Ѷȣ�һ��
4��ѡ���� ������CO2����ͨ��������Һ�У�������������������ǣ�������
A������Na2CO3��Һ
B��CaCl2��Һ
C��Na2SiO3��Һ
D��Ca��ClO��2��Һ
�ο��𰸣�A������̼���Ƶ��ܽ�ȴ���̼�����Ƶ��ܽ�ȣ���̼������Һ
���������
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ�������ӷ�Ӧ������������ԭ��Ӧ����
A.NaCl��Һ��AgNO3��Һ��Ӧ
B.Fe�ڴ�����ȼ��
C.�ڿ����е�ȼCO
D.Al��ϡ���ᷴӦ
�ο��𰸣�D
���������Aѡ������Ǹ��ֽⷴӦ��������������ԭ��Ӧ��B��C�����Ϊ�����������ķ�Ӧ�����������ӷ�Ӧ��Dѡ������������Ӳμӵ��û���Ӧ��һ��Ҳ����������ԭ��Ӧ��
�����Ѷȣ���
|