微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 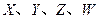 是周期表中原子序数依次增大的前20号元素。
是周期表中原子序数依次增大的前20号元素。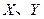 同周期。
同周期。 同主族,
同主族,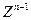 与
与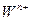 离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下
离子的电子层结构相同。由这四种元素形成的单质、化合物有如下图转化关系。已知:常温下 为液体,
为液体,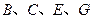 为气态化合物,且
为气态化合物,且 均为直线型分子;
均为直线型分子;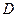 是由元素
是由元素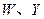 形成的常见化合物。
形成的常见化合物。
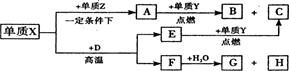
(1)元素W的名称?????,Z的原子结构示意图?????,A的电子式??????。
(2)写出D、E的化学式:D?????????、E????????????。
(3)①已知38gA与Y完全反应生成B、C时放出口aKJ的热量,写出该反应的热化学
方程式:?????????????????????????????????????????????????????????
②F与水反应的化学方程式:???????????????????????????????????????????
参考答案:
(1)钙? 本题解析:
本题解析:
本题难度:简单
2、填空题 (12分)A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含有42mol电子。回答下列问题:
(1)E元素在周期表中的位置???????;化合物M中含有的化学键类型有???????????????
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是(用化学式表示):?????;写出C与A形成的18e-化合物的电子式????????????;
(3)用电子式表示A2C的形成过程:???????????????????????????????????????
(4)写出题中生成M的化学方程式????????????????????????????????
参考答案:(1)第三周期第ⅣA族;离子键、(极性)共价键;(2)H2O
本题解析:
本题难度:一般
3、填空题 (10分)有A、B、C、D、E、F六种短周期元素,原子序数依次增大,且分属于四个主族。已知A的一种核素的原子核只有质子,B原子的最外层电子数是次外层电子数的2倍。B原子的最外层电子数是D、E原子最外层电子数之和,C原子的最外层电子数是D、F原子最外层电子数之和。请回答下列问题:
(1) 写出由A、B两种元素组成的具有10个电子的分子的电子式??????????
(2) 用电子式表示A与D形成化合物的过程?????????????????????????;
(3) A、B、C、D、E、F原子半径由大到小的顺序为??????????????????????????????,
(4) B、C、F氢化物稳定性由强到弱的顺序为???????????????????????(用化学式表示),
(5) 写出一个化学方程式证明B和C的非金属性强弱??????????????????????????????。
参考答案:(1) 本题解析:
本题解析:
本题难度:一般
4、填空题 (12分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y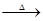 Z+W
Z+W
(1)Z的空间构型为???????????。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是?????。
(3)1mol气态Z与O2反应生成液态W和一种由两种元素组成的气体物质,放出的热量为QkJ,写出该反应的热化学方程式:???????????????????????????。
(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
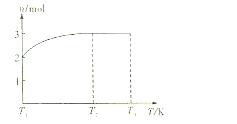
①温度在T1―T2之间,反应的化学方程式是:?????????。
②温度在T2―T3之间,气体的平均相对分子质量是(保留1位小数)????????。
③若将实验所得的平衡 混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气????????L。(设空气组成为:N2与O2,体积比4:1)
混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气????????L。(设空气组成为:N2与O2,体积比4:1)
参考答案:
 本题解析:
本题解析:
本题难度:简单
5、选择题 3He可以作为核聚变材料,以下关于3He的说法正确的是
A.比4He少一个质子
B.比4He多一个中子
C.是44He的同素异形体
D.是4He的同位素
参考答案:D
本题解析:
本题难度:简单