微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某可逆反应可设计为一新型可充放电电池,电池总反应如下:

下列说法正确的是(???)
A.放电过程中,正极附近溶液的pH变小
B.放电时,负极反应为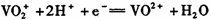
C.充电时,阳极附近溶液由绿色逐渐变为紫色
D.当电池无法放电时,只要更换电解质溶液,不用外接电源进行充电就可正常工作
参考答案:D
本题解析:放电过程的电极反应式为:正极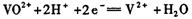 ;负极电极反应式为:
;负极电极反应式为: ;充电过程的电极反应式为:
;充电过程的电极反应式为:
阴极 本题难度:一般
本题难度:一般
2、选择题 目前,科学家正在研究开发一种高能电池--钠硫电池,它以熔融钠、硫为两极,以导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na+xS?Na2Sx,以下说法正确的是( )
A.放电时,Na作正极,S极发生还原反应
B.充电时,钠极与外电源的正极相连
C.放电时,阳极发生的反应为:S
?
2-x
-2e=xS
D.若用此电池电解AgNO3溶液,当阳极产生标准状况下的气体1.12L时,消耗的金属钠为4.6g
参考答案:A、在放电时,硫单质得电子,作正极,钠失电子,作负极,故A错
本题解析:
本题难度:简单
3、选择题 下列有关以KOH溶液为电解液的氢氧燃料电池的叙述不正确的是
A.正极反应式为:O2 + 2H2O +4e- =4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移
参考答案:B
本题解析:
试题分析:A、原电池中负极失去电子,正极得到电子,则氧气在正极通入,电极反应式为O2 + 2H2O +4e- =4OH-,A正确;B、工作一段时间后,溶剂水增加,因此电解液中KOH的物质的量浓度减小,B错误;C、该燃料电池的总反应式为:2H2+O2=2H2O,C正确;D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)即0.1mol氯气时,根据阳极电极反应式2Cl--2e-=Cl2↑可知有0.2mol电子转移,D正确,答案选B。
考点:考查电化学原理的应用
本题难度:一般
4、简答题 (14分)目前“低碳经济”备受关注。CO2的产生及有效开发利用成为科学家研究的重要课题。试利用所学知识,解决下列问题。
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: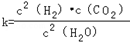 它所对应的化学反应为:_________________
它所对应的化学反应为:_________________
(2)一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如表所示:
容器
| 容积/L
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需的时间/min
|
C(s)
| H2O(g)
| H2(g)
|
甲
| 2
| T1
| 2
| 4
| 3.2
| 8
|
乙
| 1
| T2
| 1
| 2
| 1.2
| 3
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填选项字母).
A.=0.8mol?L
参考答案:
本题解析:
本题难度:困难
5、选择题 我国首创以铝―空气―海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是???????,负极反应为???????????????????????????????;正极材料是?????????,正极反应为?????????????????????????????????????。
参考答案:铝为负极,电极反应式为4Al → 4Al3++12e-,正极
本题解析:由铝―空气―海水电池靠空气中的氧气使铝不断氧化而产生电流可知,铝为负极,电极反应式为4Al → 4Al3++12e-,正极为石墨等惰性电极,反应为3O2+6H2O+12e-→ 12OH-。
本题难度:简单
|