微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 实验室要配制0.5mol/L的NaOH溶液100mL,则:
(1)需要固体NaOH的质量为______;
(2)用托盘天平称量NaOH固体时,必须把NaOH放在______仪器中称量;
(3)配制时还需要用到的仪器有______(填字母)
A.烧杯 ?B.铁架台(带铁夹)???C.100mL容量瓶???D.50mL容量瓶? E.蒸馏烧瓶????F.胶头滴管??????G.玻璃棒
(4)按实验先后顺序排列下列实验步骤______(填编号)
①将称量好的NaOH固体倒入烧杯中;
②往烧杯中倒入约20mL蒸馏水;
③将溶解并冷却后的NaOH溶液移入容量瓶;
④向容量瓶中加蒸馏水到液面离瓶颈刻度线下1~2cm;
⑤用适量蒸馏水洗涤烧杯和玻璃棒2~3次;
⑥将洗涤后的溶液也注入容量瓶中;
⑦盖好瓶塞,反复上下颠倒、摇匀;
⑧用胶头滴管滴加蒸馏水至液面与瓶颈刻度线相切.
(5)以下因素会造成所配制的NaOH溶液物质的量浓度果偏低的是______
A.NaOH溶液未经冷却后马上转移入容量瓶中
B.定容后发现液面低于刻度线补加蒸馏水
C.有少量NaOH溶液残留在烧杯中
D.容量瓶中原来有少量蒸馏水
(6)为检验精盐纯度,需配制250mL?0.2mol/L?NaCl(精盐)溶液,右图是该同学转移溶液的示意图,其中的错误是______.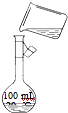
2、选择题 下列物质中所含分子物质的量最大的是( )
A.标准状况下22.4LCl2
B.56gN2
C.1.5molO2
D.3.01×1023个硫酸分子
3、选择题 硫酸钾和硫酸铝的混合溶液,已知其中Al3+的浓度为0.4mol/L,硫酸根离子浓度为0.7mol/L,则K+的物质的量浓度为( )
A.0.1mol/L
B.0.15mol/L
C.0.3mol/L
D.0.2mol/L
4、选择题 青花瓷,俗称青花,是中国瓷器的主流品种之一.某同学利用如下方法来粗略测定如图所示的青花瓷瓶的容积.把32.76g?NaCl晶体放入到500ml烧杯中,加入200ml蒸馏水,待NaCl完全溶解后,将溶液全部转移到该瓶中,用蒸馏水稀释至完全充满容器.从中取出100ml溶液,该溶液恰好能与10ml、0.100mol/L的AgNO3溶液完全反应.则下列说法正确的是( )
A.该青花瓷瓶的容积约为5.6L
B.常温下,该青花瓷瓶几乎能容纳56kgH2O
C.常温常压下,该青花瓷瓶几乎能容纳70gN2
D.青花为高级瓷器,该青花瓷瓶可以盛装氢氟酸

5、填空题 硫酸的工业制备是一个重要的化工生产过程,但在生产过程中会产生大量污染,需要在生产工艺中考虑到绿色工艺。
I尾气的吸收和综合利用。
以工业制硫酸的尾气、氨水、石灰石、焦炭、碳酸氯铵和KCI为原料可以合成硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
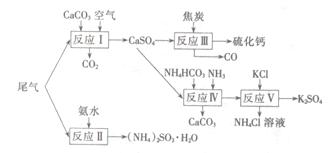
(1)反应III中氧化剂与还原剂的物质的量之比为????????????。
(2)反应Ⅳ的化学方程式为??????????????????????。
(3)反应V在25℃、40%的乙二醇溶液中进行,该反应能顺利进行的原因为???????????。
Ⅱ催化剂的回收利用。
SO2的催化氧化所使用的催化剂为V2O5,实际生产中,催化剂在使用一段时间后,会含有V2O5、VOSO4和SiO2等,其中VOSO4。能溶于水。回收V2O5,的主要流程如下:
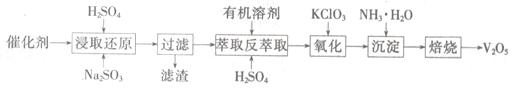
(4)若反萃取使用的硫酸用量过大,进一步处理时会增加____???????的用量。
(5)浸取还原过程的产物之一是VOSO4,反应的化学方程式为??????????????????。
氧化过程的化学方程式为KClO3+6VOSO4+3H2SO4= 2(VO)2(SO4)3+KCl+3H2O;若两步所用试剂Na2SO3与KC1O3的物质的量之比为12:7,则该催化剂中V2O5、VOSO4的物质的量之比为???????????????。