微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在稀氨水中存在下述电离平衡NH3+H2O NH3 ・H2O
NH3 ・H2O NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
加入的物质
| 少量(NH4)2SO4固体
| 少量HNO3溶液
| 少量KOH溶液
|
c(OH-)的变化
| ?
| ?
| ?
|
平衡移动方向
| ?
| ?
| ?
?
参考答案:
逆向
正向
逆向
减小
减小
本题解析:
试题分析:氨水中存在NH3+H2O NH3?H2O NH3?H2O NH4++OH-,向氨水中加入少量硫酸铵,硫酸铵电离出铵根 NH4++OH-,向氨水中加入少量硫酸铵,硫酸铵电离出铵根
本题难度:一般
2、填空题 (7分)下图为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线,试回答:
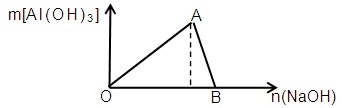
(1) A点时已参加反应的AlCl3和NaOH的物质的量之比是???????????
(2) OA段曲线所表示的反应的离子方程式是???????????????????????????
(3) AB段曲线所表示的反应的离子方程式是????????????????????????????????
(4) B处溶液中存在的浓度最大的离子是???????(填离子符号)。向B处于生成的溶液中通入CO2,可见到的现象是??????????????????????????
参考答案:(7分)
⑴ 1:3(1分)
⑵ Al3++3O
本题解析:略
本题难度:一般
3、选择题 已知HClO是比H2CO3还弱的酸,反应:Cl2+H2O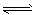 HCl+HClO,达到平衡后要使HClO的浓度增大,可加入[???? ] HCl+HClO,达到平衡后要使HClO的浓度增大,可加入[???? ]
A.Na2SO3
B.HCl ?
C.CaCO3
D.NaOH(固体)
参考答案:C
本题解析:
本题难度:一般
4、选择题 液氨与水相似,也存在着微弱的自偶电离:2NH3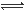 NH4++NH2-。对该体系的说法中错误的是 NH4++NH2-。对该体系的说法中错误的是
A.一定温度下,液氨中c(NH4+)与c(NH2-)的乘积为一常数
B.只要不加入其他物质,液氨中c(NH4+)总是与c(NH2-)相等
C.液氨的电离达到平衡时,c(NH3)=c(NH2-)=c(NH4+)
D.液氨中含有NH3、NH4+和NH2-
参考答案:C
本题解析:
试题分析:一定温度下,液氨中c(NH4+)与c(NH2-)的乘积就是该平衡的平衡常数,A正确;c(NH4+)和c(NH2-)按1
本题难度:一般
5、选择题 下列能说明酸HA为弱电解质的是
A.HA能与水以任意比互溶
B.常温下,0.1 mol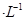 HA溶液的pH =2 HA溶液的pH =2
C.HA溶液能与Na2CO3溶液反应,产生CO2气体
D.等体积、等物质的量浓度的HA溶液和NaOH溶液恰好完全反应
参考答案:B
本题解析:
试题分析:物质在水中的溶解能力是其物理性质,而HA是否是弱电解质是其化学性质,A项不能说明,0.1mol・L-1的HA,如果是强酸,则完全电离,PH=7,实际上PH=2,溶液中的氢离子浓度为0.01mol・L-1,部分电离,B项能说明;HA的溶液能与碳酸钠溶液反应生成CO2,只能说明HA的酸性强于碳酸,C项不能说明HA是强酸,酸无论强弱,酸都能和碱发生中和反应,D项不能说明;选B。
考点:考查弱电解质强弱的判断。
本题难度:一般
|