微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于0.1mol˙L-1?Na2CO3溶液,下列说法正确的是
A.升高温度,溶液的pH降低
B.c(Na+)=2c(CO32-)+ c(HCO3-)+ c(H2CO3)
C.c(Na+)+c(H+)= 2? c(CO32-)+ 2c(HCO3-)+ c(OH-)
D.加入少量NaOH固体,c(CO32-)与c(Na+)均增大
参考答案:D
本题解析:碳酸钠水解显碱性,水解吸热,升高温度,促进水解,pH增大,A不正确。B不正确,不符合物料守恒,应该是c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)。C不正确,应该是c(Na+)+c(H+)= 2? c(CO32-)+ c(HCO3-)+ c(OH-)。加入氢氧化钠抑制水解,c(CO32-)与c(Na+)均增大,D正确,答案选D。
本题难度:一般
2、选择题 25℃时,某浓度的NH4Cl溶液pH = 4,下列叙述正确的是
A.溶液中的 c(OH-) = 1×10-10 mol·L-1
B.溶液中的c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.溶液中的c(H+) + c(NH4+) = c(Cl-) + c(OH-)
D.溶液中的c(NH3·H2O) = c(NH4+)
参考答案:AC
本题解析:
试题分析:A.NH4Cl溶液pH = 4,c(H+)=10-4mol/L.由于在25℃时Kw=10-14,所以溶液中的 c(OH-) = Kw÷c(H+)=1×10-10 mol/L。正确。B.NH4Cl是强酸弱碱盐,弱碱根NH4+离子发生水解反应而消耗,所以c(Cl-) >c(NH4+);弱碱根NH4+离子发生水解反应消耗水电离产生的OH-,使水的电离平衡被破坏,水继续电离,当最终达到电离平衡时,c(H+)>c(OH-)。盐水解的程度是很微弱的,因此c(NH4+)>c(H+)。故整个溶液中离子浓度关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-)。错误。C.根据电荷守恒可知溶液中的c(H+) + c(NH4+) = c(Cl-) + c(OH-)。正确。D.在溶液中NH3·H2O 是盐水解产生的,而NH4+是盐电离产生的。在溶液中盐水解的程度是很微弱的,因此c(NH3·H2O) <<c(NH4+)。错误。
考点:考查盐的水解在溶液中离子浓度的大小比较中的应用的知识。
本题难度:一般
3、选择题 实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是
A.防止硫酸铁分解
B.抑制硫酸铁水解?
C.提高硫酸铁的溶解度
D.提高溶液的PH
参考答案:B
本题解析:试题分析:硫酸铁溶于水,铁离子水解,溶液显酸性,所以实验操作的目的是抑制硫酸铁水解,答案选B。
考点:考查外界条件对盐类水解的影响
点评:该题是高考中的常见题型,属于等难度的试题。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练。该题的关键是明确硫酸铁的水解特点,然后结合题意和勒夏特列原理灵活运用即可,有利于培养学生的逻辑推理能力和应试能力。
本题难度:困难
4、选择题 现有1.0 mol/L的NaOH溶液0.1L,若通入标准状况下体积为2.24L 的SO2气体,使其充分反应后,则所得溶液中各粒子浓度大小关系正确的是
A.c(Na+)+c(H+) = c(HSO3
参考答案:
本题解析:
本题难度:困难
5、选择题 常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,下列对所得溶液的描述不正确的是
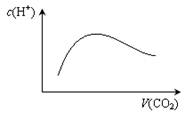
A.当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系
B.当a=b时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
C.当2a=b时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
D.当1/2<a/b<1时,所得溶液中一定存在:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
参考答案:D
本题解析:
试题分析:A、当a=2b时,二氧化碳过量,随着CO2气体的通入,先发生CO2+2NaOH=Na2CO3+H2O,生成的碳酸钠水解,促进水的电离,而氢氧化钠溶液中,氢氧根离子抑制水的电离,所以水电离产生的氢离子浓度增大,后发生Na2CO3+H2O+ CO2="2" NaHCO3,碳酸氢钠的水解程度比碳酸钠水解程度弱,所以促进水电离的程度减小,氢离子浓度又降低,符合图像,正确;B、当a=b时,所得溶液是碳酸氢钠溶液,根据质子守恒定律,水电离产生的氢离子等于氢氧根离子浓度,水电离产生的氢离子一部分被碳酸氢根离子结合生成碳酸分子,同时碳酸氢根离子电离产生氢离子和碳酸根离子,所以溶液中c(OH-)= c(H+)+c(H2CO3)- c(CO32-),即c(OH-)+c(CO32-)=c(H+)+c(H2CO3),正确;C、当2a=b时,所得溶液为碳酸钠溶液,碳酸根离子水解使溶液呈碱性,所以c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),正确;D、当1/2<a/b<1时,所得溶液为碳酸钠和碳酸氢钠的混合液,若为碳酸氢钠溶液,则一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),错误,答案选D。
考点:考查二氧化碳与氢氧化钠溶液反应的判断,离子浓度关系的判断
本题难度:一般