��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����������ʵ�����ɳ�����չ����Ҫ��������FeS2��ȼ�ղ�����SO2ͨ�����е�ѭ�����չ��̼�����H2SO4��������H2��
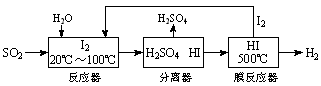
��ش��������⣺
(1) ��֪1 g FeS2��ȫȼ�շų�7.1 kJ������FeS2ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ____________________________________________________��
(2) ��ѭ�����չ��̵��ܷ�Ӧ����ʽΪ______________________________________��
(3) �û�ѧƽ���ƶ���ԭ����������HI�ֽⷴӦ��ʹ��Ĥ��Ӧ�������H2��Ŀ����___________________________________________________________________________��
(4) ������H2���ϡ������Ͻ���Ϊ��ظ������ϣ���MH��ʾ����NiO(OH)��Ϊ����������ϣ�KOH��Һ��Ϊ�������Һ�����Ƶø��������������������ء���س�ŵ�ʱ���ܷ�ӦΪ�� NiO(OH)+MH Ni(OH)2+M
Ni(OH)2+M
�ٵ�طŵ�ʱ�������ĵ缫��ӦʽΪ_________________________________��
�ڳ�����ʱ��Ni(OH)2ȫ��ת��ΪNiO(OH)����������罫��һ���缫����O2��O2��ɢ����һ���缫�����缫��Ӧ�����ģ��Ӷ�������������������ر�ը����ʱ�������ĵ缫��ӦʽΪ___________________________________��
2������� ���ܱ������м����Ũ�ȵ�CO��H2O��T ��ʱ�������·�Ӧ��CO(g)��H2O(g)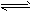 CO2��H2(g) ��H<0
CO2��H2(g) ��H<0
��֪CO��Ũ�ȱ仯��ͼ��ʾ��
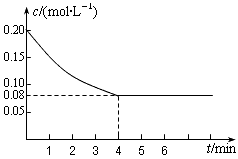
��1����0~4min���÷�Ӧ��ƽ������v(CO)��_________mol/(L��min)���÷�Ӧ��ƽ�ⳣ��Ϊ___________��
��2��Ϊ������CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��_________��
a������Ӧ����CO��Ũ��
b�����ͷ�Ӧ�¶�
c�����ܱ��������ѹ����һ��
d���������˵Ĵ���
��3�������ı䷴Ӧ�¶Ⱥͷ�Ӧ����CO����ʼŨ�ȣ�ʹCO��ת���ʴﵽ90%����ˮ��������ʼŨ������Ϊ_________mol/L��
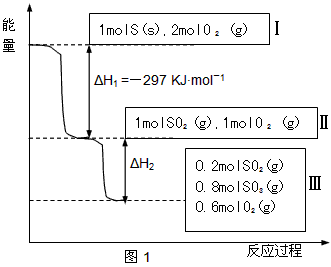
3������� ���º��������£�����Է�������ת�����䷴Ӧ���̺�������ϵ��ͼ1��ʾ������֪��
2SO2(g)+O2(g)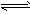 2SO3(g) ��H= ��196��6 KJ��mol-1��
2SO3(g) ��H= ��196��6 KJ��mol-1��
��ش���������
��1��д���ܱ�ʾ���ȼ���ȵ��Ȼ�ѧ����ʽ��____________________________��
��2����H2=_____________KJ��mol-1
��3�����º���ʱ��1molSO2��2molO2��ַ�Ӧ���ų���������ֵ�ȨO��H2 �O__________ (���С������ȡ�)
��4�������еĻ������ͨ��������NaOH��Һ������NaOH�����ʵ���Ϊ______________������Һ�з�����������ԭ��Ӧ����ù��̵����ӷ���ʽΪ______________________��
��5�����������£����д�ʩ����ʹn(SO3)/ n(SO2 )�������_______________��
a�������¶ȣ� b������He�� c���ٳ���1molSO2(g)��1molO2 (g) d��ʹ�ô���
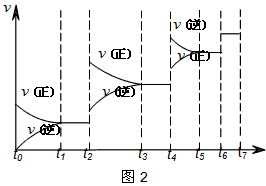
��6��ijSO2(g)��O2(g)��ϵ��ʱ��t1�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��t�Ĺ�ϵ��ͼ2��ʾ�������ı�SO2(g)��O2(g)��������ͼ��t4ʱ����ƽ���ƶ�������������__________________��ͼ�б�ʾƽ��������SO3�ĺ�����ߵ�һ��ʱ����________________________��
4��ѡ���� ����ͬ�������£�����˵��������ǣ�������
A�������ڱ��ͺ�ʳ��ˮ�е��ܽ��С���ڴ�ˮ�е��ܽ��
B�����ڶ���̼�е��ܽ�ȴ����ھƾ��е��ܽ��
C��NH3H2O��NH4Cl��Һ�е���ij̶ȴ����ڴ�ˮ�е���ij̶�
D����ҵ����������Ĺ�����ʹ�ù����Ŀ��������SO2��������
5��ѡ���� һ�������£����Ϊ10L���ܱ������У�1mol X��1mol Y���з�Ӧ�� 2X (g)+Y (g)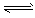 Z(g)����30s�ﵽƽ�⣬����0.3mol Z������˵����ȷ���� [???? ]
Z(g)����30s�ﵽƽ�⣬����0.3mol Z������˵����ȷ���� [???? ]
A����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.02mol/(L��S)
B�������������Ϊ20L��Z��ƽ��Ũ�ȱ�Ϊԭ����1/2
C��������ѹǿ��������Y��ת���ʼ�С
D���������¶ȣ�X�����������С����÷�Ӧ�ġ�H��0