��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ݱ�������ѧ�������о������������п���ȡ��Ǧ���أ����ط�ӦʽΪ
2Zn + O2="=" 2ZnO��ԭ����п�ϡ��������Һ��������������������ȷ���ǣ�????��
A��Zn�ǵ�ص�����
B��������Ӧ��Zn ��2e--="=" Zn2+
C����������������Ӧ
D���������ҺӦѡ��ϡ����
�ο��𰸣�B
�����������ԭ����и���ʧȥ���ʱ�����������������Ӧ�������õ����ӣ�����ԭ��������ԭ��Ӧ���ڷ�Ӧ2Zn + O2="=" 2ZnO��п�ǻ�ԭ����������������������п�Ǹ�������Ϊ����п����Һ���ᣬ���Ե���ʲ�����ϡ���ᡣ��ѡB��
�����Ѷȣ�һ��
2������� ��10�֣�Ǧ�����ǻ�ѧ��Դ����缫���Ϸֱ���Pb��PbO2���������ҺΪϡ���ᡣ����ʱ���õ�ص��ܷ�ӦΪPbO2+Pb+2H2SO4=2PbSO4+2H2O������������жϣ�
��1�����صĸ�����______����缫��ӦʽΪ______��
��2�����ص�������______����缫��ӦʽΪ______��
��3�����ع���ʱ�����е������Һ��pH______������С�����䣩��
��4��ʵ������Ǧ��������Դ��ⱥ��ʳ��ˮ��ȡ�����������Ƶ�Cl2?0.050mol����ʱ��������ĵ�H2SO4�����ʵ���������????????��
�ο��𰸣�
��1��Pb? Pb - 2e- +SO42��=PbS
������������ܷ�Ӧ�е�Ԫ�ػ��ϼ۵�������֪
Pb�ڸ���ʧ���ӣ�Pb - 2e- +SO42��=PbSO4
PbO2�������õ��ӣ�PbO2 + 4H++SO4 +2e-=PbSO4 + 2H2O
��ع��������У��������ᣬ�������Һ�����Լ�����pH����
��4�����ʳ��ˮ��2NaCl��2H2O=2NaOH��H2����Cl2�������Ƶ�0.050mol����ʱ����·�е��ӵ�ת��Ϊ0.1mol�����ڵ���ڲ�����Ӧ������������ת�ƣ����ض�����������0.1mol
�����Ѷȣ���
3��ѡ���� �ҹ��½���ij��������ʾ��ͼ��ͼ����֪Ǧ���طŵ�ʱ���ܷ�ӦΪ��Pb+PbO2+2H2SO4 = 2PbSO4+2H2O�������й�˵����ȷ����
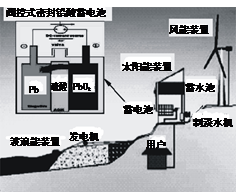
A��ͼ���漰������ת����ʽֻ��3��
B�����ع���ʱ�������ĵ缫��ӦΪ��Pb +SO42�D��2e��=PbSO4
C������ʱ�����ʱ������������������������������H2
D���÷��繤�տ�ʵ�����ŷ�
�ο��𰸣�BD
���������A�������漰������-���ܡ�̫����-���ܡ�������-��е��-���ܡ���ѧ������ܵ�����ת��
B����ȷ
C���������������岻����������������ȷ
D����ȷ
��BD
�����Ѷȣ�һ��
4��ѡ���� ���ڻ�ѧ��Դ������,�������(? )��
A����ѧ��Դ���Ǹ���ԭ��صĹ���ԭ����Ƶ�
B���ڸɵ����,̼��ֻ������,�����μӻ�ѧ��Ӧ
C�����ӵ�ز������ⶪ������Ҫԭ���������ӵ���Դ����,�۸�
D��ȼ�ϵ����һ�ָ�Ч�����������ͻ�ѧ��Դ
�ο��𰸣�C
������������ӵ�ز������ⶪ������Ҫԭ���������������ؽ���,��Ի���������ص���Ⱦ��
�����Ѷȣ�һ��
5��ѡ���� ����ȼ�ϵ�������ں���ɻ�����30%KOH��ҺΪ����ʵ����ֵ����ʹ��ʱ�ĵ缫��Ӧ���£�2H2+4OH--4e-
�ο��𰸣�
���������
�����Ѷȣ�һ��