微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供。因其独特的放电方式,也称呼吸式电池。负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液。中间设有用于隔开正极和负极的锂离子固体电解质。正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合。如图所示。下列说法不正确的是
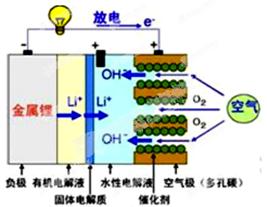
A.负极反应:Li-e-=Li+,金属锂以锂离子(Li+)的形式溶于有机电解液,电子供应给导线。溶解的锂离子(Li+)穿过固体电解质移到正极的水性电解液中。
B.正极反应:O2+2H2O+4e- =4OH-,在正极的水性电解液中与锂离子(Li+)结合生成水溶性氢氧化锂(LiOH),并能实现锂元素的循环。
C.在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开,以防止两电解液发生混合,而且能促进电池发生反应。
D.锂-空气电池至今都未普及,原因是它存在致命缺陷,即固体反应生成物氧化锂(Li2O)在正极堆积,使电解液与空气的接触被阻断,从而导致放电停止。
参考答案:D
本题解析:
试题分析:A、根据离子移动方向可知,锂失电子发生氧化反应而作负极,电极反应式为Li-e-=Li+,金属锂以锂离子(Li+)的形式溶于有机电解液,电子供应给导线.溶解的锂离子(Li+)穿过固体电解质移到正极的水性电解液中,正确;B、正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4e-=4OH-,在正极的水性电解液中与锂离子(Li+)结合生成水溶性氢氧化锂(LiOH),并能实现锂元素的循环,正确;C、锂和水反应生成氢氧化锂和氢气,所以不能让金属锂与水性电解液直接接触,在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开,以防止两电解液发生混合,而且能促进电池发生反应,正确;D、在锂-空气电池中,由于放电反应生成的并非是固体的Li2O,而是容易溶解在水性电解液中的LiOH,错误,答案选D。
考点:考查原电池和电解池原理,正负极的判断
本题难度:困难
2、填空题 常见铅蓄电池是二次电池,其电极材料分别为Pb和PbO2,电解液为稀H2SO4溶液,工作时的总反应式为Pb +PbO2+ 2H2SO4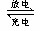 ?2PbSO4?+2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是???????????????。
?2PbSO4?+2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是???????????????。
⑵请依据两极材料和总反应,写出放电时正极反应是??????????????????????????。
⑶请依据总反应式和正极反应式,写出放电时负极反应是???????????????????????。
⑷放电时,电解质溶液中阴离子移向?????极;电流方向从?????极流向?????极。
⑸放电时,电解质溶液的酸性????????(填“增强”、“减弱”或“不变”)。
⑹充电时PbO2极发生????????反应,电极反应式??????????????????????????????;Pb极发生??????????反应,电极反应式????????????????????????????????。
参考答案::⑴铅(Pb);⑵PbO2+4H++SO42-+2e-=Pb
本题解析:此题考查几种常见电池的工作原理,结合各电极反应式及其总反应式解答。依据原电池的反应原理、铅蓄电池的工作原理及其总反应式可得答案。
本题难度:一般
3、填空题 (5分),(1)以甲烷为燃料制作新型燃料电池,电解质为氢氧化钾溶液。电池负反应式为?????????????;放电时钾离子移向电池的????????????????????????????????????????????(填“正”或“负”)????????极
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液pH=5.60,c(H2CO3)=1.5×10-5 mol・L-1。若忽略水的电离及H2CO3的第二级电离,
则H2CO3  HCO3-+H+的平衡常数K1=???????????(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=???????????(已知10-5.60=2.5×10-6)
(3)常温下,0.1 mol・L-1NaHCO3溶液的pH大于8,则溶液中
c(H2CO3)??????c(CO32-)(填“>”、“=”或“<”),原因是
???????????????????(用离子方程式和必要的文字说明)。
参考答案:(8分)(1)CH4-8e-+10OH-=CO32-+7H2
本题解析:略
本题难度:简单
4、填空题 (12分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼―空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
肼―空气燃料电池放电时:
负极的电极反应式是 ;
正极的电极反应式是 。
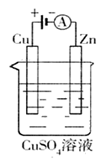
(3)下图是一个电化学过程示意图。
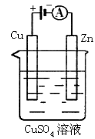
①锌片上发生的电极反应是 。
②假设使用肼―空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
参考答案:(1)N2H4(1)+O2(g) =N2(g)+2H2O(1
本题解析:
本题难度:困难
5、填空题 (15分)如图所示的装置,X、Y都是惰性电极。将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色。试回答下列问题:
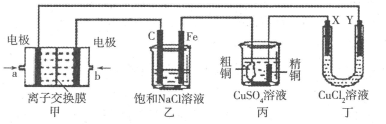
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是_______(填“CH4”或“O2”),b处电极上发生的电极反应式是____;
(2)在(乙)装置中,石墨(C)电极上发生_______反应(填“氧化”或“还原”);(乙)装置中总反应的离子方程式是:___________________________________.
(3)如果(丙)装置中精铜电极的质量增加了6.4g,则(乙)装置中,铁电极上产生的气体在标准状况下为____,(甲)装置中消耗的 CH4的质量为____。
(4)(丁)装置中X电极为_______极(填“正”、“负”、“阳”、“阴”),在通电一段时间后,Y电极上发生的电极反应式是_______。
参考答案:(1)CH4O2+2H2O+4e-=4OH-(2)氧化2Cl
本题解析:
试题分析:(1)因为甲为原电池,乙为电解池,因为铁电极附近显红色,说明是溶液中的氢离子放点,铁电极为阴极,则甲中a极为负极,甲烷在负极反应。B为原电池的正极,氧气得到电子生成了氢氧根离子,电极反应为:O2+2H2O+4e-=4OH-。(2)乙中石墨为电解池的阳极,发生氧化反应,乙中是电解氯化钠生成氢氧化钠和氯气和氢气,离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑。(3)如果精炼铜的电极上质量增加了6.4克,即为0.1摩尔铜,根据电子守恒,所以铁电极上氯离子失去0.2摩尔电子,生成标准状况下氯气的体积为2.24L,则消耗甲烷0.025摩尔,即0.025×16=0.4g。(4)丁中x连接的是原电池的正极,所以为阳极,y为阴极,y极上是溶液中的铜离子得到电子生成铜,电极反应为:Cu2++2e-=Cu。
2OH-+H2↑+Cl2↑。(3)如果精炼铜的电极上质量增加了6.4克,即为0.1摩尔铜,根据电子守恒,所以铁电极上氯离子失去0.2摩尔电子,生成标准状况下氯气的体积为2.24L,则消耗甲烷0.025摩尔,即0.025×16=0.4g。(4)丁中x连接的是原电池的正极,所以为阳极,y为阴极,y极上是溶液中的铜离子得到电子生成铜,电极反应为:Cu2++2e-=Cu。
考点:原电池的原理和电解池的原理的应用。
本题难度:困难