微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)碳及其化合物有广泛的用途。
(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作????极。
(2)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)=CO(g)+H2(g);△H=+131.3kJ?mol-1,则要制备标准状况下22.4升水煤气,转移的电子的物质的量为???,需要吸收的热量为?????????kJ。
(3)工业上把水煤气中的混合气体经过处理后,获得的较纯H2用于合成氨:
N2(g)+3H2(g) 2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
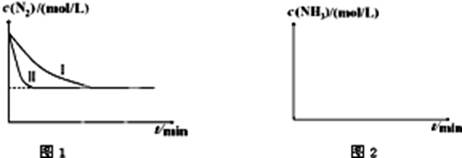
①与实验Ⅰ比较,实验Ⅱ改变的条件为:????????????????????????。
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在上图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图。
(4)Na2CO3可在降低温室气体排放中用作CO2的捕捉剂。1L0.2mol/L Na2CO3溶液吸收标准状况下2.24LCO2后,溶液中各离子浓度由大到小的顺序为???????????。
参考答案:(1)正;???(2)1mol ;65.65KJ?;
本题解析:
试题分析:(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作正极,Zn皮作负极。(2)根据反应方程式可知:每产生2mol的水煤气,转移电子2mol。现在要制备标准状况下22.4升水煤气,即制取1mol气体,所以转移的电子的物质的量为1mol;需要吸收的热量为131.3KJ÷2=65.65KJ;(3)①与实验Ⅰ比较,实验Ⅱ达到平衡所需要的时间缩短,但是平衡时物质的浓度没变,因此改变的条件为:使用催化剂。②若其它条件相同,实验Ⅲ比实验Ⅰ的温度要高,由于升高温度,化学反应速率加快,所以达到平衡所
本题难度:一般
2、选择题 现有反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的
实验
| 反应温度/℃
| Na2S2O3溶液
| 稀H2SO4
| H2O
|
V/mL
| c/(mol?L-1)
| V/mL
| c/(mol?L-1)
| V/mL
|
A
| 25
| 5
| 0.1
| 10
| 0.1
| 5
|
B
| 25
| 5
| 0.2
| 5
| 0.2
| 10
|
C
| 35
| 5
| 0.1
| 10
| 0.1
| 5
|
D
| 35
| 5
| 0.2
| 5
| 0.2
| 10
参考答案:D
本题解析:
试题分析:温度越高、浓度越大,则反应速率就越快,在实验中就最先出现浑浊。因35℃>25℃,则选项C和D中的反应速率大于选项A和B中,又D中反应物的浓度大于C中反应物的浓度,则D中反应速率最快,即在实验中就最先出现浑浊,故选D。
考点:考查影响化学反应速率的因素
本题难度:一般
3、选择题 下列条件下的反应,放出H2最快的是:( )
| 金属(粉末状)/mol | 酸的浓度和体积(mL) | 反应温度
①
Mg
0.1
3mol/LH2SO4
10
20℃
②
Al
0.1
3mol/LHCl
10
20℃
③
Zn
0.1
???3mol/LCH3COOH
10
20℃
④
Fe
0.1
6mol/LHNO3
10
20℃
A.①
B.②
C.③
D.④
参考答案:因决定化学速率的因素是反应物本身的性质,在上述金属中镁的活泼
本题解析:
本题难度:简单
4、选择题 影响化学反应速率的因素很多,下列措施一定能使化学反应速率增大的是 [???? ]
A.升高温度
B.增大压强
C.降低浓度
D.减小压强
参考答案:A
本题解析:
本题难度:一般
5、选择题 把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )。
A.盐酸的浓度
B.铝条的表面积
C.溶液的温度
D.加少量Na2SO4
参考答案:D
本题解析:本题主要考查影响化学反应速率的条件。应熟记影响反应速率的因素及分别会产生怎样的影响。除反应物的本身外,影响反应速率的外界条件有多种,如浓度、温度、压强、催化剂、反应物的表面积、光照等。因此A、B、C项均能影响产生H2的速率。而加入少量Na2SO4与反应无关。故正确答案为D。
本题难度:简单
|
|