��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��16�֣�(1)��һ�鴿����пƬ����ʢ��ϡ������ձ���ɹ۲쵽пƬ���ܽ⣬���������������ƽ�еز���һ��ͭƬ����ͼ����ʾ�����ɹ۲쵽ͭƬ�� ����С���û�С������ݲ��������õ��߰�пƬ��ͭƬ������������ͼ����ʾ�����ɹ۲쵽ͭƬ�ϣ���С���û�С��� ���ݲ�����
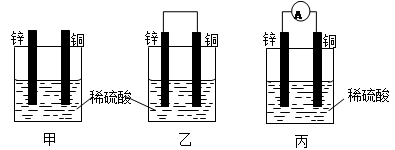
��2���õ����������������������˺�������Һ�е�пƬ��ͭƬ��������ͼ����ʾ�����۲쵽������������ָ�뷢����ƫת��˵���˵������е���ͨ���������������п��Թ��ɳ�����ԭ��ص�һЩ������ ��
�йصĵ缫��Ӧʽ��пƬ ��ͭƬ ��
ͼ����ʾԭ����У���������Ϊ ��
��3��ͼ�ҡ�ͼ����һ���� ��ת��Ϊ �ܵ�װ�ã����ǰ�������ԭ��ء�
�ο��𰸣���1��û�У�2�֣����У�2�֣���
��2�����缫Ҫ�����
�������������ԭ��ص�Ӧ�ü����жϡ�ͭ�ڽ����˳�����������ĺ��棬���Ժ�ϡ�����Ӧ�����õ��ߺ�п����������ϡ�����У���ԭ��أ�п�Ǹ�����ʧȥ���ӣ�����������Ӧ��ͭ�����������Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ������������������õ����ӣ�������ԭ��Ӧ�������������缫��ӦʽΪ������Zn��2e����Zn2+��������2H+ + 2e�� =H2�����������Ϸ�����֪������ԭ��ص������ǻ����Բ�ͬ�Ľ����������ǽ�������������������Ҫ����������Һ�С�ԭ����ǰѻ�ѧ��ת��Ϊ���ܵ�װ�á�
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ�������
A�����MgCl2������Һ�����Ƶý���þ
B�����س��ʱ���为��Ӧ���Դ����������
C�����ִ�������п�鱣����Dz��ܸ�ʴ�Dz�������������������
D���������ڿ�����¶���������绯ѧ��ʴ�����䰵
�ο��𰸣�A�����õ�����ڵ��Ȼ�þ��ұ������Mg�������MgCl2����
���������
�����Ѷȣ�һ��
3������� ���й���ԭ��ص������У�������ǣ�������
A��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ��
B���õ������ӵ����ֲ�ͬ����ͬʱ����Һ���У������γ�ԭ���
C����ԭ����У������ϣ����·�����ӵ��磬��Һ�У��ڵ�·�����ӵ���
D����ԭ����У�����������һ���Ǹ���������������Ӧ
�ο��𰸣�A��ԭ����ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã���A��ȷ��
B��
���������
�����Ѷȣ�һ��
4������� ��пƬ��ͭƬ���Ӻ����ϡ������Һ�У�������ԭ��أ�����һ��ʱ�䣬пƬ������������3.25�ˣ�ͭ��������������______L����״���£���������ͨ��______mol���ӣ�
�ο��𰸣���пƬ��ͭƬ���Ӻ����ϡ������Һ�У�������ԭ��أ�
п
���������
�����Ѷȣ���
5������� (8��)����ݷ�Ӧ��Fe + Cu2+? =? Fe 2++ Cu ���ԭ��أ�
(1)???(2��)����ʵ��ļ���װ��ͼ������Ǧ�ʻ�ͼ��
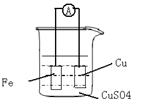
(2)(6��)д���缫��Ӧʽ��������???????????????????��������?????????????????������Ӧ���е�һ��ʱ���ȡ���缫���ϣ����ijһ�缫������6.4g,��Ӧ��ת���˵ĵ�������???????????��
�ο��𰸣�(2)? Cu2+ + 2e- = Cu???
������������ý�����Fe������Fe �C 2e- = Fe2+???Cu(��) Cu2+ + 2e- = Cu??
0.4mol?? 0.2mol??? NA=0.2NA=1.204��1023
�����Ѷȣ�һ��