��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ʵ�в����õ绯ѧ���۽��͵��� [???? ]
A.��Щ����ˮբ��ˮ�����²���Ƕ��п��
B.���Ͻ��Ŵ�����Ϳˢ����
C.ʵ����������ʱ�ô�п���ô�п�ų�������
D.�Ʋ������п���ȶ�������ʴ
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� ������ʵ�����õ绯ѧ���۽��͵���
A���Ʋ㱻���ƺ�п������Ʒ�ȶ���������Ʒ��ʴ
B���ִ�ˮ�����µĴ�������Ƕ��һ������п��
C����Ƭ�������ⷽ������
D��п��ϡ���ᷴӦʱ��������������ͭ��Һ��Ӧ���ʼӿ�
�ο��𰸣�C
���������
�����������������Zn��Fe��Sn������ѡ��A��ȷ�����ڽ����ĵ绯ѧ��ʴ�������B������������������������C�����ǻ��õĽ�����������������γ�һ�����ܵı���Ĥ��������ʴ�ԣ����͵绯ѧ�أ�D��п�ܰ�����ͭ�е�ͭ�����û���ͭ���Ӷ�����ͭпԭ��أ��ӿ췴Ӧ���ʣ���ѡC��
�������������е��Ѷȵ����⣬�����������У���Ҫ�ǿ��������Ե绯ѧԭ�����˽�̶ȣ��Լ�������õ绯ѧ���ʵ�����������������������ѧ������˼ά������
�����Ѷȣ���
3��ѡ���� ijС��Ϊ�о��绯ѧԭ�����������ͼװ�á�����������ȷ���ǣ�????��

A��a��b�õ�������ʱ����Ƭ�ϻ��н���ͭ����
B��a��b�õ�������ʱ��ͭƬ�Ϸ����ķ�ӦΪ��Cu2����2e�D = Cu
C������a��b�Ƿ����ӣ���Ƭ�����ܽ�
D������a��b�Ƿ����ӣ���Ƭ�Ϸ����ķ�Ӧ���ǣ�Fe ��3e�D =Fe3��
�ο��𰸣�C
���������a��b�õ�������ʱ������ԭ��أ����Ǹ�����ͭ����������Һ�е�ͭ�����������õ����Ӷ�����ͭ���ʣ�A��B����ȷ��a��b�����ӣ�����ֱ�Ӻ�����ͭ�����û���Ӧ������C��ȷ��D����ȷ��Ӧ����Fe ��2e�D =Fe2������ѡC��
�����Ѷȣ�һ��
4��ѡ���� ����ʵ��װ�÷���ʵ��Ŀ����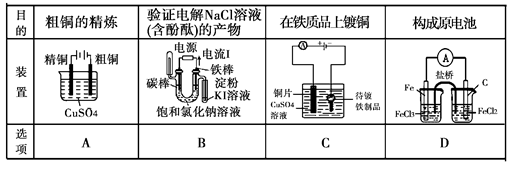
�ο��𰸣�C
���������
���������A����ͭ�ľ���Ӧ���Ǵ�ͭ��Ϊ���������ӵ�ص�������B�����ʳ��ˮ��Һ�������������������������������������ƣ�ͼ�е�̼��һ���������������Լ�������Ӧ�ý����۵⻯����Һ����̼��һ����C��ȷ��D����װ�ò����γ�ԭ��أ���Ӧ�ý����ߵĵ������Һ�Ի��ſ����γ�ԭ��ء�
���������⿼����ԭ��أ����ص�֪ʶ����Щ��������Ϊ�߿�������ص���ѵ㣬������һ�����ۺ��ԣ��Ѷ����С�
�����Ѷȣ�һ��
5������� ��Ҫ����գ�
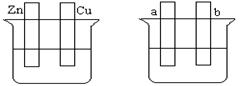
A??????????????????? B
��1����Aͼ�У�ϡ����Ϊ�������Һ���õ������Ӻ�ͭƬ�缫��Ӧʽ????????��
��2����Bͼ�����ֱ����Դ����Ҫ��a����ͭ�����Ա�Ҫ�����Ӻ�װ�ý�????????��b���缫��Ӧʽ????????????????????????????????????��
��3����Bͼ�����ֱ����Դ�����缫Ϊ���Ե缫���������Һ��CuSO4��Һ��������������ܷ�Ӧ���ӷ���ʽΪ????????????????????????����������3.2 g���������Ϸų��������ڱ�״���µ������_____L������һ������?????���ѧʽ������Һ�ָܻ�������ǰ��ȫһ�¡�
�ο��𰸣���1��2H+ +2e=H2��
��2����Ƴػ��ƣ�Cu
���������
�����������1��A��ӦΪпͭԭ��أ�п��������Zn2+������Һ��������пƬͨ����������ͭƬ����Һ�е�H+��ͭƬ��õ��ӣ�����ԭ����ԭ�ӡ���ԭ�ӽ�ϳ�����Ӵ�ͭƬ�Ϸų��������������·�Ӧ��������Zn-2e-=Zn2+??������ 2H+ +2e=H2��??ͭƬ�ϵķ�ӦΪ��2H+ +2e=H2��
��2����Ƶ�����Ϊ����Դ���缫������ʡ��պϻ�·������������ָ��Ҫ��a����ͭ�����Դ�װ��Ϊ��Ƴء�Ҫ��a����ͭ����ôa���������ǻ�ԭ��Ӧ��b����������������Ӧ���缫��Ӧ����ʽΪ��Cu - 2e- = Cu
�����Ѷȣ�һ��